题目内容
(1)工业上用电解饱和NaCl溶液的方法生产氯气,NaCl溶于水发生电离的方程式为 .
(2)2004年4月15日,某化工厂发生氯气泄漏事件,工作人员喷射NaOH人员形成液幕,保卫并吸收泄漏的氯气,其反应方程式为 .
(3)事件过后,附近居民向记者反映当时晾在外面的衣服褪色了,其原因是 .
(2)2004年4月15日,某化工厂发生氯气泄漏事件,工作人员喷射NaOH人员形成液幕,保卫并吸收泄漏的氯气,其反应方程式为
(3)事件过后,附近居民向记者反映当时晾在外面的衣服褪色了,其原因是
考点:电离方程式的书写,氯气的化学性质
专题:元素及其化合物
分析:(1)氯化钠是强电解质,在水溶液里电离出阴阳离子;
(2)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(3)氯气和水反应生成次氯酸,次氯酸有漂白性;
(2)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(3)氯气和水反应生成次氯酸,次氯酸有漂白性;
解答:
解:(1)氯化钠是强电解质,在水分子作用下完全电离出阴阳离子,所以其电离方程式为:NaCl=Na++Cl-,
故答案为:NaCl=Na++Cl-;
(2)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的化学方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,离子反应方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2NaOH═NaCl+NaClO+H2O;
(3)氯气和水反应生成次氯酸,反应方程式为:Cl2+H2O?HCl+HClO,HClO具有强氧化性,可漂白,所以能使湿衣服褪色,
故答案为:Cl2+H2O?HCl+HClO,HClO具有强氧化性,可漂白有色物质;
故答案为:NaCl=Na++Cl-;
(2)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的化学方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,离子反应方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2NaOH═NaCl+NaClO+H2O;
(3)氯气和水反应生成次氯酸,反应方程式为:Cl2+H2O?HCl+HClO,HClO具有强氧化性,可漂白,所以能使湿衣服褪色,
故答案为:Cl2+H2O?HCl+HClO,HClO具有强氧化性,可漂白有色物质;
点评:本题考查了电解质的电离、方程式书写,注意掌握氯气与碱溶液反应的方程式,明确具有漂白性的是次氯酸,不是氯气.题目难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
下列物质不能通过单质间化合反应制取的是( )
| A、Na2O2 |
| B、FeCl2 |
| C、SO2 |
| D、HCl |
有反应4HCl+O2→2Cl2+2H2O,已知2molO2被还原时,放出a kJ的热量,且知断开1mol
O2需要吸收b kJ的热量,断开1molCl2需要吸收c kJ的热量.则断开1mol H-O键比断开1molH-Cl 键所需能量高( )
O2需要吸收b kJ的热量,断开1molCl2需要吸收c kJ的热量.则断开1mol H-O键比断开1molH-Cl 键所需能量高( )
A、
| ||
B、
| ||
C、
| ||
D、
|
已知NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A、氯化铁溶液加热蒸干最终得不到氯化铁固体 |
| B、镀锡的铁制品,镀层部分受损后,露出的铁表面更易被腐蚀 |
| C、电解精炼铜时,每转移2 mol电子阳极上溶解的铜原子数为NA |
| D、在lL0.lmol.L-1碳酸钠溶液中,阴离子总数大于0.1NA |
下列说法正确的是( )
| A、摩尔是国际单位制中的七个物理量之一 |
| B、摩尔表示物质的量 |
| C、1mol任何物质都含有6.02×1023个原子 |
| D、1mol O2中有6.02×1023个氧分子 |
下列说法不正确的是( )
| A、12C、13C、14C 为碳元素的三种核素.元素周期表中碳的相对原子质量为12.01,说明自然界中的碳主要以12C的核素形式存在.14C为放射性核素,可用于同位素示踪 |
| B、汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率 |
| C、能量是可以互相转化的.植物的光合作用可将太阳能转变成化学能,单晶硅可将光能转变成电能.原电池和电解池可实现化学能和电能的相互转化 |
| D、乳酸分子中既有羟基又有羧基,因此可在一定条件下缩聚得到聚乳酸(PLA).该高分子化合物是一种可降解的环保材料 |
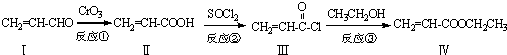
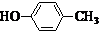 也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为