题目内容
配制0.1mol?L-1的CuSO4溶液时,下列情况会导致所配溶液的实际浓度偏高的是( )
| A、定容时仰视容量瓶的刻度线 |
| B、容量瓶没有烘干 |
| C、托盘天平的砝码生锈 |
| D、定容时加水多后用滴管吸出 |
考点:溶液的配制
专题:实验评价题
分析:分析不当操作对溶质物质的量和溶液体积的影响,依据C=
进行误差分析.
| n |
| V |
解答:
解:A.定容时仰视容量瓶的刻度线,导致溶液的体积偏大,溶液的浓度偏低,故A不选;
B.容量瓶没有烘干对溶质物质的量和溶液体积都不会产生影响,溶液的浓度不变,故B不选;
C.砝码生锈后增重,使称量的固体质量偏大,溶质的物质的量偏大,所配溶液的浓度偏高,故C选;
D.定容时加水多后用滴管吸出,导致溶质的物质的量偏小,溶液的浓度偏低,故D不选;
故选:C.
B.容量瓶没有烘干对溶质物质的量和溶液体积都不会产生影响,溶液的浓度不变,故B不选;
C.砝码生锈后增重,使称量的固体质量偏大,溶质的物质的量偏大,所配溶液的浓度偏高,故C选;
D.定容时加水多后用滴管吸出,导致溶质的物质的量偏小,溶液的浓度偏低,故D不选;
故选:C.
点评:本题考查了配制一定物质的 浓度溶液的误差分析,准确判断不当操作对溶质的物质的量和溶液体积的影响是解题关键,题目难度不大.

练习册系列答案
相关题目
已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ?mol-1,OH-(aq)+H+(aq)═H2O(l)△H=-57.3kJ?mol-1,则下列说法正确的是( )
| A、2 mol CH4在足量的氧气中充分燃烧生成稳定的氧化物的燃烧热为-1780.6 kJ?mol-1 |
| B、2 mol CH4在足量的氧气中充分燃烧生成CO2(g)和H2O(g)的燃烧热为-890.3 kJ?mol-1 |
| C、1 L 0.1 mol?L-1 NaOH溶液与1 L 0.1 mol?L-1 HCl溶液反应的中和热为-57.3 kJ?mol-1 |
| D、2 L 1 mol?L-1 NaOH溶液与1 L 1 mol?L-1 H2SO4溶液反应的反应热为-57.3 kJ?mol-1 |
只用一种试剂,便能把浓度均为1mol/L的Na2SO3、Na2SO4、Na2CO3、Na2S、Na2SiO3五种溶液区别开来的是( )
| A、CaCl2溶液 |
| B、AgNO3溶液 |
| C、NaOH溶液 |
| D、稀H2SO4 |
 香花石是中国地质学家发现的第一种世界新矿物,被誉为中国矿石的“国宝”,其化学式为Ca3Li2(BeSiO4)F4.下列说法中不正确的是( )
香花石是中国地质学家发现的第一种世界新矿物,被誉为中国矿石的“国宝”,其化学式为Ca3Li2(BeSiO4)F4.下列说法中不正确的是( )| A、原子半径:Li>Be>O>F |
| B、气态氢化物的稳定性:SiH4<H2O<HF |
| C、最高价氧化物对应水化物的碱性:Ca(OH)2>LiOH>Be(OH)2 |
| D、CaO2、SiO2两种化合物中氧元素的化合价相同 |
1993年我国学者和美国科学家首先合成了两种大分子的烃C1134H1146和C1398H1278,在合成相对分子质量为2000~5000,并且具有确定结构的有机化合物这个新的研究领域中处于领先地位.C1134H1146可能具有的性质是( )
| A、常温下呈液态 |
| B、性质稳定,不易被氧化 |
| C、能发生加成反应 |
| D、有极高的硬度 |

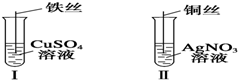 按如图所示操作,充分反应后:
按如图所示操作,充分反应后: 25℃时,已知某些物质的电离平衡常数如表:
25℃时,已知某些物质的电离平衡常数如表: