题目内容
20.一定条件下,将1mol X气体和1mol Y气体充人一1L的恒容密闭容器中,发生反应:X(g)+2Y(g)?3Z(g),1s后测得c(Y)=0.6mol•I-1,则0~1s内Y的平均反应速率为( )| A. | 0.2 mol•L-l•s-l | B. | 0.4 mol•L-l•s-l | C. | 0.6 mol•L-l•s-l | D. | 0.8 mol•L-l•s-l |
分析 1s后测得c(Y)=0.6mol•I-1,则转化的Y为1mol/L-0.6mol/L=0.4mol/L,结合v=$\frac{△c}{△t}$计算.
解答 解:1s后测得c(Y)=0.6mol•I-1,则转化的Y为1mol/L-0.6mol/L=0.4mol/L,可知0~1s内Y的平均反应速率为$\frac{0.4mol/L}{1s}$=0.4 mol•L-l•s-l,
故选B.
点评 本题考查化学反应速率,为高频考点,把握反应中浓度的变化量、速率计算为解答的关键,侧重分析与应用能力的考查,注意速率计算公式的应用,题目难度不大.

练习册系列答案
相关题目
10.下列说法中正确的是( )
| A. | 锂离子电池和普通锌锰干电池都是二次电池 | |
| B. | 原电池的反应的本质是氧化还原反应 | |
| C. | 燃料电池是一种高效但是会污染环境的新型电池 | |
| D. | 铅蓄电池放电的时候正极是Pb负极是PbO2 |
11.下列说法不正确的是( )
| A. | 在25℃时,将amol•L-1的氨水与0.01 mol•L-1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),用含a的代数式表示NH3•H2O的电离常数:Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
| B. | 在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应生成Z,平衡后测得X、Y的转化率与起始时两物质的物质的量之比n(X)/n(Y>的关系如图所示,则x与Y的反应方程式可表示为:X+3Y?nZ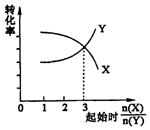 | |
| C. | 某同学在实验室进行了如图所示的实验,则Y中反应的离子方程式为:3CaCO3+2Fe3++3H2O═2Fe(OH)3+3CO2↑+3Ca2+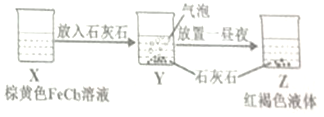 | |
| D. | 将10mL 1 mol•L-1Na2CO3溶液逐滴滴加到10mL1mol•L-1盐酸中,滴加结束后生成的溶液中有:C(Na+)>c(Cl-)>c(CO32-)>c(HCO3-) |
8.下列有关σ键和π键的说法错误的是( )
| A. | 在某些分子中,化学键可能只有σ键而没有π键 | |
| B. | 分子中σ键的键能一定大于π键的键能 | |
| C. | σ键的特征是轴对称,π键的特征是镜面对称 | |
| D. | SO2形成π键与O3的π键是相似的 |
15.下列关于有机化合物的说法正确的是( )
| A. | 乙酸和乙酸乙酯可用Na2CO3溶液加以区别 | |
| B. | 卤代烃和醇都可以发生消去 | |
| C. | 乙烯、聚氯乙烯和苯分子均含有碳碳双键 | |
| D. | 卤代烃、酯及酚均可发生水解反应 |
5.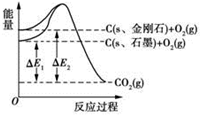 2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地.1mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )
2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地.1mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )
 2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地.1mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )
2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地.1mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )| A. | 1 mol石墨完全转化为金刚石需吸收1.9 kJ的能量 | |
| B. | 石墨转化为金刚石属于物理变化 | |
| C. | 金刚石的稳定性强于石墨的 | |
| D. | 1 mol金刚石的能量大于1mol CO2的能量 |
9.对下列物质的类別与所含官能团判断中,不正确的是( )
| A. | 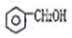 醇类-OH 醇类-OH | B. | CH3CH2COOH 羧酸类-COOH | ||
| C. | 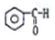 酮类-CHO 酮类-CHO | D. | CH3CH2Br 卤代烃类-Br |
19.下列关于碱金属、卤族元素的说法正确的是( )
| A. | 碱金属单质的失电子能力随着原子序数的增加而减小 | |
| B. | 从上到下,卤素原子的电子层数依次增多,半径依次减小 | |
| C. | 从F到I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱 | |
| D. | 碱金属单质都是强氧化剂 |
 .
.