题目内容
 硼酸钛[(TiO)2(B2O5)?4H2O]是一种高效节能润滑油添加剂,可用硫酸氧钛和硼砂的溶液为原料湿法合成.
硼酸钛[(TiO)2(B2O5)?4H2O]是一种高效节能润滑油添加剂,可用硫酸氧钛和硼砂的溶液为原料湿法合成.(1)基态Ti原子的电子排布式为
(2)硫酸氧钛中Ti元素的化合价与硼酸钛中相同,且带有2个结晶水.硫酸氧钛的化学式为
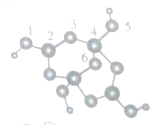
(3)硼砂是含结晶水的四硼酸钠,其阴离Xm-(含B、O、H三种元素)的球棍模型.如图所示:
①在Xm-中,硼原子轨道的杂化类型有
②硼砂晶体由Na+、Xm-和H2O构成,硼砂晶体中存在的作用力有
A.离子键 B.共价键 C.金属键 D.氢键 E.范德华力.
考点:原子核外电子排布,配合物的成键情况,原子轨道杂化方式及杂化类型判断,不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:(1)Ti的原子序数为22,核外有22个电子;
(2)根据化合价的代数和为零计算Ti的化合价,再写出硫酸氧钛的化学式;
(3)①1,3,5,6形成两个共价键代表氧原子,2,4形成三个共价键代表B原子,2号B形成3个键,则B原子为SP2杂化,4号B形成4个键,则B原子为SP3杂化; B一般是形成3个键,4号B形成4个键,其中1个键很可能就是配位键,配位键存在4号与5号之间,结合化合价代数和为0的原则判断;
②注意题目要求,钠离子与Xm-形成离子键,结晶水分子间存在氢键和范德华力.
(2)根据化合价的代数和为零计算Ti的化合价,再写出硫酸氧钛的化学式;
(3)①1,3,5,6形成两个共价键代表氧原子,2,4形成三个共价键代表B原子,2号B形成3个键,则B原子为SP2杂化,4号B形成4个键,则B原子为SP3杂化; B一般是形成3个键,4号B形成4个键,其中1个键很可能就是配位键,配位键存在4号与5号之间,结合化合价代数和为0的原则判断;
②注意题目要求,钠离子与Xm-形成离子键,结晶水分子间存在氢键和范德华力.
解答:
解:(1)①Ti的原子序数为22,核外有22个电子,其电子排布为[Ar]3d24s2,故答案为:[Ar]3d24s2;
(2)设硼酸钛[(TiO)2(B2O5)?4H2O]中Ti为+x价,则(x-2)×2+3×2+(-2)×5=0,则x=4,即硫酸氧钛中钛为+4价,则硫酸氧钛的化学式为TiOSO4?2H2O;
故答案为:TiOSO4?2H2O;
(3)①1,3,5,6形成两个共价键代表氧原子,2,4形成三个共价键代表B原子,2号B形成3个键,则B原子为SP2杂化,4号B形成4个键,则B原子为SP3杂化; B一般是形成3个键,4号B形成4个键,其中1个键很可能就是配位键,配位键存在4号与5号之间.观察模型,可知Xm-是(H4B4O9)m-,依据化合价H为+1,B为+3,O为-2,可得m=2,
故答案为:sp2、sp3;4,5;2;
②钠离子与Xm-形成离子键,结晶水分子间存在氢键和范德华力,故答案为:ADE.
(2)设硼酸钛[(TiO)2(B2O5)?4H2O]中Ti为+x价,则(x-2)×2+3×2+(-2)×5=0,则x=4,即硫酸氧钛中钛为+4价,则硫酸氧钛的化学式为TiOSO4?2H2O;
故答案为:TiOSO4?2H2O;
(3)①1,3,5,6形成两个共价键代表氧原子,2,4形成三个共价键代表B原子,2号B形成3个键,则B原子为SP2杂化,4号B形成4个键,则B原子为SP3杂化; B一般是形成3个键,4号B形成4个键,其中1个键很可能就是配位键,配位键存在4号与5号之间.观察模型,可知Xm-是(H4B4O9)m-,依据化合价H为+1,B为+3,O为-2,可得m=2,
故答案为:sp2、sp3;4,5;2;
②钠离子与Xm-形成离子键,结晶水分子间存在氢键和范德华力,故答案为:ADE.
点评:本题考查了电子排布式、化学式、杂化类型的判断、化学键和分子间作用力等,题目难度中等,侧重于基础知识的综合应用的考查.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
我国城市近年来已发布“空气质量日报”.下列物质中不列入首要污染物的是( )
| A、NO2 |
| B、SO2 |
| C、CO2 |
| D、可吸入颗粒物 |
下列有关阿伏加德罗常数(NA)的说法错误的是( )
| A、32 g氧气和臭氧的混合气体中所含的原子数为2N. |
| B、常温常压下,22.4LCO2含有的分子数目为NA |
| C、0.1mol OH-含有NA个电子 |
| D、2.4g金属镁与足量的盐酸反应,转移的电子数为0.2NA |
下列反应的能量变化与其他三项不相同的是( )
| A、铝粉与氧化铁的反应 |
| B、NH4Cl晶体与Ba(OH)2?8H2O晶体的反应 |
| C、锌片与稀硫酸反应 |
| D、钠与冷水反应 |
用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术.已知反应Fe2O3+3Na2O2
2Na2FeO4+Na2O,下列说法正确的是( )
| ||
| A、Na2O2既是氧化剂又是还原剂 |
| B、Na2FeO4既是氧化产物又是还原产物 |
| C、3 mol Na2O2发生反应,有12mol 电子转移 |
| D、在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌 |
下列反应的离子方程式正确的是( )
| A、NaHCO3溶液与盐酸:CO32-+2 H+=H2O+CO2↑ |
| B、实验室制二氧化碳:CaCO3+2H+=CO2↑+H2O+Ca2+ |
| C、向硝酸亚铁溶液中加入稀硫酸:Fe2++4H++NO3-=Fe3++NO↑+2H2O |
| D、AlCl3溶液与过量氨水反应:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
下列有机物只有四种同分异构体的是( )
| A、分子式为C4H10烷烃的二氯取代物 |
| B、分子式为C3H9N的有机物,其中N原子以三个单键与其他原子相连 |
| C、乙苯的二氯取代物 |
| D、分子式为C4H8的有机物 |