题目内容
9.下列指定微粒的数目相等的是( )| A. | 等物质的量的H2O与D2O含有的中子数 | |
| B. | 等质量的SO2和SO3中含有氧原子数 | |
| C. | 同温同压下,同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别于足量氯气完全反应时转移的电子数 |
分析 A.1个H2O与1个D2O含有的中子数不同;
B.依据n=$\frac{m}{M}$结合1个二氧化硫含有2个氧原子,1个三氧化硫含有3个氧原子解答;
C.一氧化碳和NO含有的质子数不同;
D.铁、铝与氯气反应生成氯化铁和氯化铝;
解答 解:A.1个H2O与1个D2O含有的中子数不同,所以等物质的量的H2O与D2O含有的中子数不相同,故A错误;
B.等质量的SO2和SO3中含有氧原子数分别为:$\frac{m}{64}$×2=$\frac{m}{32}$,$\frac{m}{80}$×3=$\frac{3m}{80}$,二者不相等,故B错误;
C.CO的质子数为6+8=14,而NO的质子数为7+8=15,同温、同压、同体积的一氧化碳和NO含有的质子数不相等,故C错误;
D.铁和铝分别与足量氯气完全反应,Fe、Al元素的化合价均由0升高为+3价,则等物质的量的铁和铝分别与足量氯气完全反应时转移的电子数均为n×(3-0)NA,故D正确;
故选:D.
点评 本题考查物质的量的计算,为高频考点,把握物质的构成、物质的量计算公式、转移电子计算等为解答的关键,侧重分析与应用能力、计算能力的考查,题目难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
19.下列事实中,不能用平衡移动原理解释的是( )
| A. | 氯气中有下列平衡Cl2+H2O?HCl+HClO,当加入AgNO3(s)后溶液颜色变浅 | |
| B. | 2NO2(g)?N2O4(g)△H<0,升高温度可使体系颜色加深 | |
| C. | 反应CO+NO2?CO2+NO△H<0,升高温度可使平衡向逆反应方向移动 | |
| D. | 合成氨反应N2+3H2?2NH3△H<0,使用催化剂加快反应速率 |
20.对1mol/L的Na2SO4(摩尔质量为142g/mol)溶液的叙述中正确的是( )
| A. | 溶液中含有1mol的Na2SO4 | |
| B. | 从1L溶液中取出500 mL后,剩余溶液的浓度变为0.5mol/L | |
| C. | 1mol的Na2SO4 溶于1L水 | |
| D. | 1L溶液中含有142 g Na2SO4 |
4.某有机物的结构如图所示,下列说法不正确的是( )
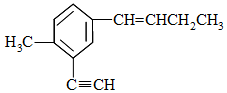

| A. | 与乙苯不互为同系物 | |
| B. | 分子中共直线的碳原子最多有4个 | |
| C. | 分子中共平面的原子最多有20个 | |
| D. | 与其互为同分异构体且萘环上只有一个侧链的共有4种 |
14.下列溶液中的c (Cl -)与100mL 1mol•L-1氯化铝溶液中的c (Cl-)相等( )
| A. | 300mL 1mol•L-1 氯化钠溶液 | B. | 150mL 2mol•L-1氯化铵溶液 | ||
| C. | 75mL 3mol•L-1 氯化钙溶液 | D. | 10mL 1.5mol•L-1 氯化钡溶液 |
1.溶液、胶体和浊液这三种分散系的本质区别是( )
| A. | 分散质的粒子是否为大量分子或离子的集合体 | |
| B. | 能否透过滤纸 | |
| C. | 分散质粒子直径的大小 | |
| D. | 是否均一、稳定 |
18.下列物质:HCHO(甲醛)、MgSO4、NH4Cl、Hg(NO3)2中,能使蛋白质变性的是( )
| A. | 甲醛 | B. | MgSO4 | C. | NH4Cl | D. | Hg(NO3)2 |