题目内容
能说明常温下二氧化硅是很坚硬的固体而二氧化碳是气体的原因是( )
| A、硅的非金属性比碳的活泼 |
| B、二氧化硅中硅氧键的类型和二氧化碳中碳氧键不同 |
| C、硅氧键的键能比碳氧键的键能大得多 |
| D、二氧化硅晶体类型和二氧化碳晶体不同 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A.非金属性强弱与其氧化物的聚集状态无关,硅的非金属性不及碳的活泼;
B.二氧化硅中硅氧键的类型和二氧化碳中碳氧键相同;
C.硅氧键的键能比碳氧键的键能小得多,且与其氧化物的聚集状态无关;
D.分子晶体是由分子通过分子间作用力结合而成的,原子晶体是由原子通过共价键以空间网状结构形成.
B.二氧化硅中硅氧键的类型和二氧化碳中碳氧键相同;
C.硅氧键的键能比碳氧键的键能小得多,且与其氧化物的聚集状态无关;
D.分子晶体是由分子通过分子间作用力结合而成的,原子晶体是由原子通过共价键以空间网状结构形成.
解答:
解:A.碳原子和硅原子最外层电子都为4,都属于第ⅣA元素,且碳在硅的上一周期,同一主族,从上往下,非金属性逐渐减弱,所以碳的非金属性强于硅,且非金属性强弱与氧化物的聚集状态无关,故A错误;
B.二氧化硅中硅氧键的类型和二氧化碳中碳氧键都为极性共价键,故B错误;
C.碳原子和硅原子最外层电子都为4,都属于第ⅣA元素,且碳在硅的上一周期,硅的原子半径大于碳,所以硅氧键的键能比碳氧键的键能小得多,且键能大小与其氧化物的聚集状态无关,聚集状态与熔点有关,与晶体类型有关,故C错误;
D.二氧化硅晶体是立体的网状结构,每个硅原子周围连有四个氧原子,每个氧原子周围连有2个硅原子,属于原子晶体,原子晶体熔点高,常温下为固态,二氧化碳为分子晶体,熔点低,常温下为气态,故D正确;
故选D.
B.二氧化硅中硅氧键的类型和二氧化碳中碳氧键都为极性共价键,故B错误;
C.碳原子和硅原子最外层电子都为4,都属于第ⅣA元素,且碳在硅的上一周期,硅的原子半径大于碳,所以硅氧键的键能比碳氧键的键能小得多,且键能大小与其氧化物的聚集状态无关,聚集状态与熔点有关,与晶体类型有关,故C错误;
D.二氧化硅晶体是立体的网状结构,每个硅原子周围连有四个氧原子,每个氧原子周围连有2个硅原子,属于原子晶体,原子晶体熔点高,常温下为固态,二氧化碳为分子晶体,熔点低,常温下为气态,故D正确;
故选D.
点评:本题考查有关元素性质的知识,侧重考查晶体的类型的判断,注意非金属性强弱可以通过氢化物的稳定性判断,熔点与晶体的类型有关是解题的关键,题目难度中等.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
2mol O3和2mol H2S相比较,下列叙述中正确的是( )
| A、摩尔质量相等 | B、原子数相等 |
| C、体积相等 | D、质量相等 |
下列有关电解质溶液的叙述,不正确的是( )
| A、稀醋酸加水稀释,醋酸电离程度增大,溶液的pH升高 |
| B、在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
| C、在含有BaSO4沉淀的溶液中加入Na2SO4固体,溶液中c(Ba2+)减小 |
| D、常温下,pH=2的盐酸与pH=12的氨水等体积混合所得溶液c(H+)>c(OH-) |
常温下,已知0.1mol/L的NaX、NaY、NaZ溶液,其pH值分别为8、9、10,则HX、HY、HZ的酸性强弱排列正确的是( )
| A、HX>HY>HZ |
| B、HY>HX>HZ |
| C、HZ>HY>HX |
| D、HZ>HX>HY |
下列说法中错误的是( )
| A、缺锌会影响骨骼、牙齿的生长 |
| B、毒品是指由于非医疗目的而反复使用使人产生成瘾性的药品,如吗啡、冰毒等 |
| C、R表示处方药,OTC表示非处方药 |
| D、过量服用维生素C,会引起泌尿系统结石 |
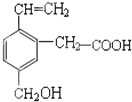 某有机物的结构为如图,该有机物不可能具有的性质是( )
某有机物的结构为如图,该有机物不可能具有的性质是( )①可以燃烧氧化;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生一个分子内或n个分子间酯化反应;
⑤能发生加聚反应;
⑥它有手性碳原子
⑦能被催化氧化成醛
⑧该有机物的碳原子存在sp2、sp3杂化.
| A、①④ | B、④⑥ | C、⑤⑦ | D、只有⑥ |
设NA表示阿伏加德罗常数的值.下列说法不正确的是( )
| A、1mol醋酸的质量与NA个醋酸分子质量相等 |
| B、NA个O2和NA个H2的质量比等于16:1 |
| C、28gN2所含的原子数目为NA |
| D、1.7gNH3所含电子数目为NA |
短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示.下列说法正确的是( )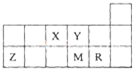

| A、元素X和M的氧化物对应的水化物均为强酸 |
| B、R的单质能与M的氢化物发生置换反应 |
| C、气态氢化物的稳定性:M>Y |
| D、元素Y、Z形成的简单离子半径大小关系为:Z>Y |