题目内容
1.2008北京奥运会圆满结束,其中“祥云”火炬燃料是丙烷(C3H8)气体.以丙烷、氧气和CO2及熔融碳酸盐可制作新型燃料电池,电池的总反应式为:C3H8+5O2═3CO2+4H2O.下列说法正确的是( )| A. | 每消耗1 mol C3H8可以向外电路提供12 mol e- | |
| B. | 负极通入C3H8,发生还原反应 | |
| C. | 正极通入氧气和CO2,正极反应式是:O2+2CO2+4e-═2CO32- | |
| D. | CO32-移向电池的正极 |
分析 负极通入丙烷,碳元素的化合价升高,发生反应:C3H8+10CO32--20e-=13CO2+4H2O,电池的正极通入O2,氧元素的化合价降低,发生反应:O2+2CO2+4e-═2CO32-,电解质溶液中阴离子向负极移动.
解答 解:A、负极通入丙烷,碳元素的化合价升高,发生反应:C3H8+10CO32--20e-=13CO2+4H2O,每消耗1 mol C3H8可以向外电路提供20mole-,故A错误;
B、负极通入丙烷,碳元素的化合价升高,发生氧化反应:C3H8+10CO32--20e-=13CO2+4H2O,故B错误;
C、正极通入氧气和CO2,发生还原反应,正极反应式是O2+2CO2+4e-═2CO32-,故C正确;
D、CO32-移向电池的负极,故D错误.
故选C.
点评 本题考查了原电池原理的应用,题目难度不大,侧重于基础知识的考查,注意把握燃料电池中电极方程式的书写方法是关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.下列叙述一定正确的是( )

| A. | 常温常压下,相同物质的量的物质,其体积一定相等 | |
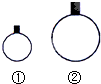
| B. | 常温常压下,用等质量的H2、CH4两种气体分别吹出如图所示的两个气球,其中①号气球内气体一定为CH4 | |
| C. | 任何条件下,等物质的量的氮气和一氧化碳所含的分子数、原子数不一定相等 | |
| D. | 1mol金属镁与其他物质发生化学反应,金属镁失去的电子数一定是2NA |
12.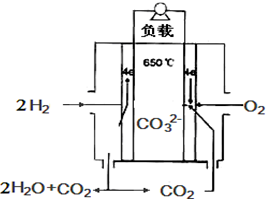 熔融碳酸盐燃料电池,是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔金属阳极、金属极板构成的燃料电池.其电解质是熔融态碳酸盐.如图是用熔融碳酸盐作电解质,氢气和氧气形成的燃料电池,下列说法不正确的是( )
熔融碳酸盐燃料电池,是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔金属阳极、金属极板构成的燃料电池.其电解质是熔融态碳酸盐.如图是用熔融碳酸盐作电解质,氢气和氧气形成的燃料电池,下列说法不正确的是( )
 熔融碳酸盐燃料电池,是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔金属阳极、金属极板构成的燃料电池.其电解质是熔融态碳酸盐.如图是用熔融碳酸盐作电解质,氢气和氧气形成的燃料电池,下列说法不正确的是( )
熔融碳酸盐燃料电池,是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔金属阳极、金属极板构成的燃料电池.其电解质是熔融态碳酸盐.如图是用熔融碳酸盐作电解质,氢气和氧气形成的燃料电池,下列说法不正确的是( )| A. | 该电池放电时,负极的反应式为:H2-2e-+CO32-═H2O+CO2 | |
| B. | 该电池中CO32-的为由左边移向右边移动 | |
| C. | 该电池放电时,正极的反应式为:O2+2CO2+4e-═2CO32- | |
| D. | 该电池放电时,当转移4mol e-时正极消耗1mol O2和2mol CO2 |
9.在溶液导电性实验装置里在相同温度下分别注入20mL 6mol•L-1醋酸和20mL6mol•L-1氨水,灯光明暗程度相同,如果把这两种溶液混和后再试验则( )
| A. | 灯光变暗;二者电离常数相同 | B. | 灯光变暗;电离常数醋酸大于氨水 | ||
| C. | 灯光变亮;电离常数醋酸小于氨水 | D. | 灯光变亮;电离常数醋酸等于氨水 |
6.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1 L 1mol/L NaHCO3溶液中自由移动的离子总数为3NA | |
| B. | 常温常压下,1.06g Na2CO3含有Na+数目为0.02NA | |
| C. | 1 mol Na2O2与CO2反应电子转移为2 NA | |
| D. | 40g NaOH溶解在1 L水中,得到溶液的物质的量浓度为1 mol/L |
11.下列关于乙酸的说法不正确的是( )
| A. | 可以除去热水瓶内胆水垢 | B. | 具有挥发性 | ||
| C. | 能与乙醇反应生成有香味的酯 | D. | 能发生加聚反应 |
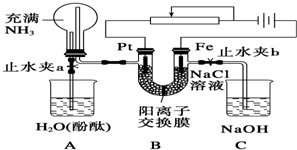
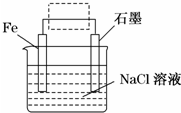 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C.(填字母)
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C.(填字母)