题目内容
下列对物质的认识或判断全部正确的一项是( )
| 物质 | 类别 | 化学键类型 | 水溶液是否导电 | 熔融态是否导电 | 是否为电解质 | |
| A | NaOH | 强碱 | 离子键 | 导电 | 导电 | 是 |
| B | HCl | 共价化合物 | 非极性键 | 导电 | 导电 | 是 |
| C | Na2S | 离子化合物 | 离子键和非极性键 | 导电 | 导电 | 是 |
| D | CO2 | 氧化物 | 共价键 | 导电 | 不导电 | 是 |
| A、A | B、B | C、C | D、D |
考点:酸、碱、盐、氧化物的概念及其相互联系,离子化合物的结构特征与性质,极性键和非极性键
专题:物质的分类专题,电离平衡与溶液的pH专题
分析:A、氢氧化钠是强碱是强电解质水溶液中或熔融状态都导电;
B、氯化氢是共价化合物水溶液中导电属于强电解质,熔融状态不导电;
C、硫化钠是盐属于离子化合物,水溶液中或熔融状态都导电,是强电解质;
D、二氧化碳是共价化合物,水溶液中能导电,是二氧化碳和水反应生成电解质碳酸,本身不能电离属于非电解质.
B、氯化氢是共价化合物水溶液中导电属于强电解质,熔融状态不导电;
C、硫化钠是盐属于离子化合物,水溶液中或熔融状态都导电,是强电解质;
D、二氧化碳是共价化合物,水溶液中能导电,是二氧化碳和水反应生成电解质碳酸,本身不能电离属于非电解质.
解答:
解:A、氢氧化钠是强碱,是强电解质,属于离子化合物含有离子键,水溶液中或熔融状态都导电,故A正确;
B、氯化氢是共价化合物,水溶液中导电属于强电解质,熔融状态不导电,含有极性共价键,故B错误;
C、硫化钠是盐属于离子化合物,水溶液中或熔融状态都导电,是强电解质,不含极性键只含离子键,故C错误;
D、二氧化碳是共价化合物,水溶液中能导电,是二氧化碳和水反应生成电解质碳酸,本身不能电离属于非电解质,故D错误;
故选A.
B、氯化氢是共价化合物,水溶液中导电属于强电解质,熔融状态不导电,含有极性共价键,故B错误;
C、硫化钠是盐属于离子化合物,水溶液中或熔融状态都导电,是强电解质,不含极性键只含离子键,故C错误;
D、二氧化碳是共价化合物,水溶液中能导电,是二氧化碳和水反应生成电解质碳酸,本身不能电离属于非电解质,故D错误;
故选A.
点评:本题考查了物质分类方法和概念实质的分析判断,掌握物质组成和性质是解题关键,题目较简单.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列有关实验结论正确的是( )
| A、某单质的水溶液能使淀粉碘化钾溶液变蓝,则该溶液一定为氯水或者溴水 |
| B、向某无色溶液中滴加氯化钡溶液,产生白色沉淀,加入稀盐酸后该沉淀不溶解,说明原溶液中一定含有SO42-离子 |
| C、向某固体中滴加稀盐酸,产生能使澄清石灰水变浑浊、但不能使品红溶液褪色的气体,则原固体中一定含有CO32-或HCO3-离子 |
| D、为测定2SO2+O2?2SO3反应混合物中硫元素的总量,将其加入到足量硫酸酸化的高锰酸钾溶液中,再加足量BaCl2溶液,过滤、洗涤、干燥、称量、计算即可 |
在下列元素中,不属于主族元素的是( )
| A、砷 | B、铍 | C、铁 | D、碘 |
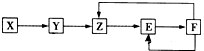 五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如图转化关系,下列推断不合理的是( )
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如图转化关系,下列推断不合理的是( )| A、M元素可能是非金属元素,也可能是金属元素 |
| B、X可能是一种氢化物 |
| C、E可能是一种有色气体 |
| D、X→Y可能是非氧化还原反应 |
常温下,在指定环境中,下列各组离子一定不可以大量共存的是( )
| A、使pH试纸呈红色或蓝色的溶液:ClO4-、SO42-、Na+ |
| B、使酚酞变红色的溶液:K+、SO32-、CO32-、SO42- |
| C、透明的溶液:Cu2+、Al3+、SO42-、Cl- |
| D、加入铝粉后产生大量氢气的溶液:NH4+、Na+、NO3-、SO42- |
根据中学化学课本中的数据资料作出以下推断,其中不正确的是( )
| A、利用密度数据可判断液体物质挥发性的大小 |
| B、利用化合价数据可以确定某些元素原子的最外层电子数 |
| C、利用原子半径数据可推断某些原子的氧化性和还原性的强弱 |
| D、利用溶解度数据可推测将一些物质混合物分离开来的可能性 |
下列化学用语正确的是( )
A、CH3COOH的球棍模型 |
B、第三周期简单阴离子结构示意图均可表示为 |
| C、HIO结构式为H-I-O |
| D、37Cl中的37代表该原子的相对原子质量 |