��Ŀ����
��10�֣� A��B��C��D����ǰ18��Ԫ����ɵ����ֳ��������DΪ����ɫ���壬�ס��������ֵ��ʣ���Щ���ʺͻ�����֮��������·�Ӧ��ϵ��
��1������ת�������а����ķ�Ӧ����Ϊ ��
a�û���Ӧ b���Ϸ�Ӧ c�ֽⷴӦ d���ֽⷴӦ
��2�����ڼ���ȼ�գ�����1 mol e��ת�ƣ�����Һ̬Aʱ�� �ų�142.9 kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��3����Ӧ����һ��������Ϊ���淴Ӧ������һ��ʱ��÷�Ӧ�ﵽƽ�⣬д���÷�Ӧ�Ļ�ѧ����ʽ�� ������3 mol��4 mol C��ϳ����ݻ�Ϊ2 L���ܱ������У�2���Ӻﵽƽ�⡣ƽ������������ʵ���Ϊ6 mol���Ļ�ѧ��Ӧ����Ϊ ������ƽ�����ﻺ��ͨ��ˮ�еõ�1L��Һ��������Һ���ʵ���Ũ����____________��
��1��b��c
��2��H2(g ) + 1/2 O2(g) = H2O(l)����H=-285.8 kJ/mol
��3��2 NO +O2 2NO2 ��0.25 mol/(L��min) ��4mol/L ��ÿ��2�֣�
����:

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ

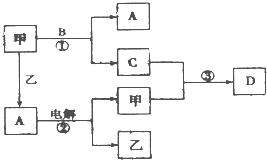 A��B��C��D���ɶ�����Ԫ����ɵ����ֳ����Ļ����DΪ����ɫ���壬�ס��������ֵ��ʣ���Щ���ʺͻ�����֮�������ͼ��ʾ��ת����ϵ��
A��B��C��D���ɶ�����Ԫ����ɵ����ֳ����Ļ����DΪ����ɫ���壬�ס��������ֵ��ʣ���Щ���ʺͻ�����֮�������ͼ��ʾ��ת����ϵ�� ��2010?������ģ��A��B��C��D����ǰ18��Ԫ����ɵ����ֳ��������DΪ����ɫ���壬�ס��������ֵ��ʣ���Щ���ʺͻ�����֮�������ͼ��Ӧ��ϵ��
��2010?������ģ��A��B��C��D����ǰ18��Ԫ����ɵ����ֳ��������DΪ����ɫ���壬�ס��������ֵ��ʣ���Щ���ʺͻ�����֮�������ͼ��Ӧ��ϵ��
