题目内容
11.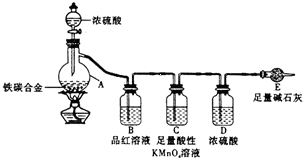 某学习小组设计了图示实验装置(省略了夹持仪器)来测定某铁碳合金中铁的质量分数.
某学习小组设计了图示实验装置(省略了夹持仪器)来测定某铁碳合金中铁的质量分数.(1)称取w g铁碳合金,加入足量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:
①常温下碳与浓硫酸不反应;②常温下Fe遇浓硫酸发生钝化.
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(3)B中的现象是:品红溶液褪色;C的作用是:除尽反应产物中的SO2气体.
(4)如果利用球形干燥管反应前后质量的变化来测定铁的质量分数,甲同学认为结果可能偏大,理由是装置内的CO2难以被E完全吸收;也可能偏小,理由是空气中的CO2和水被碱石灰吸收.
(5)乙同学认为可以用烧瓶里反应后的溶液经过一系列操作来测定铁的质量分数:加入足量的NaOH溶液、过滤、洗涤、在空气中灼烧、称重.洗涤应该在过滤装置中进行;检查是否洗净,需要用到的试剂是BaCl2溶液.一系列操作后所得固体为a g,则合金中铁的质量分数为$\frac{70a}{w}$%.
(6)丙同学认为可以用中和滴定的方法来测定铁的质量分数:将反应后烧瓶里的溶液转移至锥形瓶中,加入0.1000mol/L氢氧化钠溶液30.00mL,反应完全后,加2滴甲基橙溶液,过量的氢氧化钠用0.1000mol/L盐酸滴定至终点,耗用盐酸20.10mL.
①把标准盐酸注入润洗过的红色手柄滴定管后,应该打开活塞,使尖嘴部分充满溶液并排出气泡,并使液面位于零刻度或零刻度以下位置,记录读数.
②从物质性质的角度分析,该方法即使操作规范,也有很大的误差,其实属于“方法错误”,理由是因为溶液中可能同时有+3价和+2价的铁,无法计量,不能用甲基橙,因为酸性环境,可能造成沉淀溶解.
分析 由装置图可知,该实验原理:通过测定干燥管E的质量增重确定二氧化碳的质量,根据二氧化碳的质量计算铁碳合金中碳的质量,进而计算铁的质量,再计算合金中铁的质量分数.故二氧化硫会影响二氧化碳的测定,进入干燥管E的气体应除去二氧化硫、且干燥.
(1)常温下碳与浓硫酸不反应,铁在浓硫酸中发生钝化现象;
(2)碳与浓硫酸在加热的条件下生成二氧化硫、二氧化碳、水;
(3)A中生成的气体含有CO2、2SO2,SO2具有漂白性,能使品红溶液褪色;二氧化硫存在会影响二氧化碳的质量测定,C装置的作用为除尽反应产物中的SO2气体;
(4)装置内残留部分二氧化碳,未能被装置E完全吸收,导致测量的二氧化碳的质量偏小,即合金中碳元素的质量偏小,如果碱石灰吸收了空气中的二氧化碳和水,则导致测量的二氧化碳的质量偏大,即合金中碳元素的质量偏大;
(5)称取w g铁碳合金,加入足量浓硫酸反应生成硫酸铁,加入足量的NaOH溶液,过滤洗涤干燥,灼烧至恒重,称量得到氧化铁的质量ag,结合元素守恒和质量分数定义计算;洗涤应该在过滤装置中进行;检查是否洗净,需要用到的试剂是氯化钡溶液检验是否含有硫酸根离子;
(6)①依据滴定管使用方法和基本操作回答;
②溶液中可能同时有+3价和+2价的铁,无法计量,甲基橙变色范围是3.1--4.4属于酸性溶液,可能溶解沉淀.
解答 解:由装置图可知,该实验原理:通过测定干燥管E的质量增重确定二氧化碳的质量,根据二氧化碳的质量计算铁碳合金中碳的质量,进而计算铁的质量,再计算合金中铁的质量分数.故二氧化硫会影响二氧化碳的测定,进入干燥管E的气体应除去二氧化硫、且干燥.
(1)常温下,铁与浓硫酸反应生成一层致密的氧化物保护膜,阻止内金属继续与浓硫酸反应,发生钝化现象,
故答案为:常温下Fe遇浓硫酸发生钝化;
(2)碳与浓硫酸在加热的条件下生成二氧化硫、二氧化碳、水,反应方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(3)A中生成的气体含有CO2、2SO2,SO2具有漂白性,能使品红溶液褪色;C装置的作用为除尽反应产物中的SO2气体,防止影响二氧化碳的质量测定,
故答案为:品红溶液褪色;除尽反应产物中的SO2气体;
(4)装置内残留部分二氧化碳,未能被装置E完全吸收,导致测量的二氧化碳的质量偏小,即合金中碳元素的质量偏小,铁元素的质量偏大,质量分数偏大,也可能偏小是因为空气中的CO2和水被碱石灰吸收,则导致测量的二氧化碳的质量偏大,即合金中碳元素的质量偏大,铁元素的质量偏小,质量分数偏小;
故答案为:装置内的CO2难以被E完全吸收;空气中的CO2和水被碱石灰吸收;
(5)称取w g铁碳合金,加入足量浓硫酸反应生成硫酸铁,加入足量的NaOH溶液,过滤洗涤干燥,灼烧至恒重,称量得到氧化铁的质量ag,结合元素守恒和质量分数定义计算;洗涤应该在过滤装置中进行;检查是否洗净,需要用到的试剂是氯化钡溶液检验是否含有硫酸根离子;
合金中铁的质量分数=$\frac{\frac{ag}{160g/mol}×2×56g}{wg}$×100%=$\frac{70a}{w}$%;
故答案为:过滤、灼烧;BaCl2溶液;$\frac{70a}{w}$;
(6)①把标准盐酸注入润洗过的红色手柄滴定管后,应该打开活塞,尖嘴部分充满溶液并排出气泡,并使液面位于零刻度或零刻度以下位置,记录读数;
故答案为:尖嘴部分充满溶液并排出气泡;
②该方法即使操作规范,也有很大的误差,属于“方法错误”的理由是:因为溶液中可能同时有+3价和+2价的铁,无法计量;不能用甲基橙,因为酸性环境,可能造成沉淀溶解;
故答案为:因为溶液中可能同时有+3价和+2价的铁,无法计量,不能用甲基橙,因为酸性环境,可能造成沉淀溶解.
点评 本题考查了物质组成的分析判断,实验探究方法,滴定实验故分析应用,注意计算方法和基本操作的理解应用,掌握基础是关键,题目难度中等.

 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材(必修加选修)中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材(必修加选修)中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
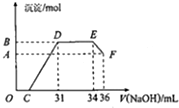
II.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示.
请回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为NH4++OH-═NH3•H2O.
(2)B与A的差值为0.008mol,B点对应的沉淀的物质的量为0.032mol,C点对应的氢氧化钠溶液的体积为7ml.
| A. | SO2中混有少量SO3,通过足量浓硫酸,收集气体 | |
| B. | HNO3溶液中混有少量H2SO4,加入适量BaCl2溶液,再过滤 | |
| C. | 提取溴水中的溴,可用加入乙醇萃取的方法 | |
| D. | 检验溶液中是否含有Fe2+,向溶液中滴入氯水后,再滴加KSCN溶液 |
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol•L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c( S2O82-)/mol•L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
(2)反应中发生反应的I-与被氧化的I-的物质的量比为3:2.
(3)该实验的目的是研究I-、S2O82-浓度对反应速率的影响;显色时间t1=22s;若c(I-)=0.64mol/L,c(S2O82-)=0.02mol/L,请估算该反应显色的时间应为11s.
| A. | 正丁烷和异丁烷的一氯取代物都只有两种,它们的沸点也相同 | |
| B. | 乙烯分子与苯分子都能与H2发生加成反应,说明二者均含碳碳双键 | |
| C. | 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应 | |
| D. | 乙醛加入Cu(OH)2粉末并加热可看到红色沉淀生成 |
①导电性;②瓦斯爆炸;③缓慢氧化;④丁达尔效应;⑤萃取;⑥焰色反应.
| A. | ①②④ | B. | ②③ | C. | ②③⑥ | D. | ②③⑤ |