题目内容
12.已知:常温下,H2CO3 Ka1=4.2×10-7,Ka2=5.6×10-11,某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者所占的物质的量分数(a)随溶液pH变化关系如图所示,下列叙述错误的是( )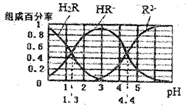
| A. | 在pH=4.4的溶液中:3c(HR-)=c(Na+)+c(H+)-c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2R溶液混合后,溶液中水的电离程度比纯水小 | |
| C. | 在pH=3的溶液中存在 $\frac{c({R}^{2-})×c({H}_{2}R)}{c(H{R}^{-})^{2}}$=10-3.1 | |
| D. | 向Na2CO3溶液中加入少量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR- |
分析 A.在pH=4.4的溶液中,c(R2-)=c(HR-),根据电荷守恒分析;
B.等体积等浓度的NaOH溶液与H2R溶液混合后,生成等浓度的H2R、HR-,溶液的pH=1.3;
C.根据Ka1=$\frac{c(H{R}^{-})×c({H}^{+})}{c({H}_{2}R)}$,Ka2=$\frac{c({R}^{2-})×c({H}^{+})}{c(H{R}^{-})}$计算;
D.根据电离常数比较酸性强弱,然后判断反应产物.
解答 解:A.在pH=4.4的溶液中,c(R2-)=c(HR-),溶液中电荷守恒为:2c(R2-)+c(HR-)+c(OH-)=c(Na+)+c(H+),所以3c(HR-)=c(Na+)+c(H+)-c(OH-),故A正确;
B.等体积等浓度的NaOH溶液与H2R溶液混合后,生成等浓度的H2R、HR-,溶液的pH=1.3,溶液显酸性,对水的电离起到抑制作用,所以溶液中水的电离程度比纯水小,故B正确;
C.当溶液pH=1.3时,c(H2R)=c(HR-),则Ka1=$\frac{c(H{R}^{-})×c({H}^{+})}{c({H}_{2}R)}$=10-1.3,溶液的pH=4.4时,c(R2-)=c(HR-),则Ka2=$\frac{c({R}^{2-})×c({H}^{+})}{c(H{R}^{-})}$=10-4.4,
$\frac{c({R}^{2-})×c({H}_{2}R)}{c(H{R}^{-})^{2}}$=$\frac{{K}_{a2}}{{K}_{a1}}$=10-3.1,故C正确;
D.由C选项分析可知,H2R的电离常数Ka2大于H2CO3的Ka2,即酸性:HR->HCO3-,所以向Na2CO3溶液中加入少量H2R溶液,发生反应:2CO32-+H2R=2HCO3-+R2-,故D错误.
故选D.
点评 本题考查了据图分析数据进行电离平衡常数的计算、电离程度与水解程度大小判断以及电荷守恒的应用,题目难度中等,侧重于考查学生的分析能力和计算能力.

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案| A. | 过氧化钠电子式: | |
| B. | 质子数35、中子数45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子结构示意图: | |
| D. | HClO的结构式:H-Cl-O |
| A. | 农作物收获后,就地焚烧秸秆,增加土壤中钾肥含量 | |
| B. | 工业废水可经过“再生”处理,用于城市道路保洁、喷泉和浇花用水 | |
| C. | 硅单质常作为制备光导纤维的主要材料 | |
| D. | 淘米水中含有淀粉可以直接检测加碘盐中是否含有碘元素 |
| A. | 铝热剂 | B. | 黑火药 | C. | 木炭 | D. | 丹药(硫化汞) |
| A. | 加入碳酸锰的目的是除去Fe3+ | |
| B. | 常温下pH=4时,Fe3+已除尽 | |
| C. | Cu2+(aq)+MnS(s)=CuS(s)+Mn2+(aq)的K=2.73×10-23 | |
| D. | Mn2(OH)2CO3、Mn(OH)2都可以替代MnCO3 |
| A. | CH3Cl只存在一种空间结构 | |
| B. | CH2Cl2只存在一种空间结构 | |
| C. | CHCl3只存在一种空间结构 | |
| D. | CH4的四个价键的键角和键长都相等 |
 .
.
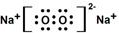 ,该物质所含有的微粒间作用力的类型为离子键、共价键.
,该物质所含有的微粒间作用力的类型为离子键、共价键.