题目内容
19.能够用键能大小解释的是( )| A. | 氮气的化学性质比氧气稳定 | |
| B. | 常温、常压下,溴呈液态,碘呈固态 | |
| C. | 稀有气体一般很难发生化学反应 | |
| D. | 相同状态下,氯气的密度比空气的大 |
分析 A.物质的稳定性与键能有关;
B.根据组成和结构相似的分子晶体,相对分子质量越大,熔点越高;
C.稀有气体为单原子分子,原子都形成稳定结构;
D.相同状态下,密度大小与体积和质量有关,与键能无关.
解答 解:A.氮气分子中N≡N的键能比氧气分子中O=O的键能强,故化学性质比氧气分子稳定,与键能有关,故A正确;
B.溴的相对分子质量比碘单质小,所以溴的沸点比碘单质低,常温、常压下,溴呈液态,碘呈固态,与键能无关,故B错误;
C.稀有气体为单原子分子,原子都形成稳定结构,稀有气体一般难于发生化学反应,与键能无关,故C错误;
D.密度ρ=$\frac{m}{v}$,相同状态下,同体积的氯气和氢气,氯气的质量大于氢气,所以氯气的密度比空气的大,与键能无关,故D错误;
故选A.
点评 本题考查化学键和分子间作用力这两个不同概念,需要注意的是物质的稳定性与键能有关,题目难度不大.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
10.对于具有相同电子层结构的三种微粒:An+、Bn-、C,下列分析正确的是( )
| A. | 原子半径:ra>rb>rc | B. | 微粒半径:Bn->An+ | ||
| C. | C元素不一定是稀有气体元素 | D. | 原子序数:C>B>A |
4.液氧是航天活动一种重要氧化剂,常与液氢或煤油等配合使用,以下说法错误的是( )
| A. | 工业通过分馏液态空气制备液氧 | |
| B. | 液氧不可燃,铁路旅客可以随身携带 | |
| C. | 液氧与液氢搭配做火箭推进剂的优点之一是清洁环保 | |
| D. | 沥青若长时间浸入液氧可能会发生爆炸 |
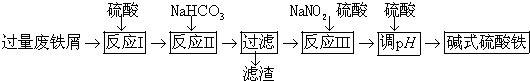
8.碱式硫酸铁[Fe(OH)SO4]可用作净水剂、媒染剂、颜料和药物.工业上利用废铁屑(含少量氧化铝、氧化铁等)生成碱式硫酸铁的部分工艺如图:
已知:部分阳离子以氢氧化物形式沉淀时溶剂的pH见表:
(1)反应Ⅰ中发生的氧化还原反应的离子方程式是Fe+2H+═Fe2++H2↑、Fe+2Fe3+═3Fe2+.
(2)反应Ⅱ中加入NaHCO3调节体系PH在4.4≤pH<7.5 范围内.
(3)反应Ⅲ中生成的气体遇空气变红棕色,则反应Ⅲ中发生反应的离子方程式是2H++Fe2++NO2-=Fe3++NO↑+H2O.
(4)反应Ⅲ中通入氧气可减少NaNO2的用量,若消耗1mol氧气可节约n(NaNO2)=4mol.
(5)用硫酸控制体系的PH,若硫酸加入量过小,容易生成沉淀;若硫酸加入量过大,不利于产品形成,用化学平衡移动原理分析其原因是过量的硫酸与Fe(OH)SO4电离出来的OH-中和,使电离平衡向右移动,不利于产物生成.
(6)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)${\;}_{4}^{2+}$聚合离子,该水解反应的离子方程式是2[Fe(OH)]2++2H2O?[Fe2(OH)4]2++2H+.

已知:部分阳离子以氢氧化物形式沉淀时溶剂的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(2)反应Ⅱ中加入NaHCO3调节体系PH在4.4≤pH<7.5 范围内.
(3)反应Ⅲ中生成的气体遇空气变红棕色,则反应Ⅲ中发生反应的离子方程式是2H++Fe2++NO2-=Fe3++NO↑+H2O.
(4)反应Ⅲ中通入氧气可减少NaNO2的用量,若消耗1mol氧气可节约n(NaNO2)=4mol.
(5)用硫酸控制体系的PH,若硫酸加入量过小,容易生成沉淀;若硫酸加入量过大,不利于产品形成,用化学平衡移动原理分析其原因是过量的硫酸与Fe(OH)SO4电离出来的OH-中和,使电离平衡向右移动,不利于产物生成.
(6)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)${\;}_{4}^{2+}$聚合离子,该水解反应的离子方程式是2[Fe(OH)]2++2H2O?[Fe2(OH)4]2++2H+.