题目内容
解释下列物质性质的变化规律与物质结构间的因果关系时,与化学键强弱无关的变化规律是( )
| A、HF、HCI、HBr、HI的热稳定性依次减弱 |
| B、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| C、F2、C12、Br2、I2的熔、沸点逐渐升高 |
| D、Li、Na、K、Rb 的熔点逐渐降低 |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:当物质发生变化时,存在化学键的断裂或生成,则与化学键有关,发生变化时只有分子间作用力的变化,则与化学键无关.
解答:
解:A.影响HF、HCl、HBr、HI稳定性的因素是化学键键能的大小,与化学键有关,故A不选;
B.NaF、NaCl、NaBr、NaI属于离子晶体,影响熔点高低的因素是离子键的强弱,与化学键有关,故B不选;
C.F2、C12、Br2、I2属于分子晶体,影响熔沸点高低的因素是分子间作用力的大小,与化学键无关,故C选;
D.Li、Na、K、Rb是金属晶体,影响熔点高低的因素是金属键的强弱,与化学键有关,故D不选;
故选C.
B.NaF、NaCl、NaBr、NaI属于离子晶体,影响熔点高低的因素是离子键的强弱,与化学键有关,故B不选;
C.F2、C12、Br2、I2属于分子晶体,影响熔沸点高低的因素是分子间作用力的大小,与化学键无关,故C选;
D.Li、Na、K、Rb是金属晶体,影响熔点高低的因素是金属键的强弱,与化学键有关,故D不选;
故选C.
点评:本题考查化学键与物质的性质之间的关系,题目难度不大,注意化学键与分子间作用力以及氢键的区别.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
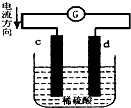 如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c、d为两个电极.则下列有关的判断不正确的是( )
如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c、d为两个电极.则下列有关的判断不正确的是( )| A、d为负极,发生氧化反应 |
| B、c为锌片,电池工作时,溶液中SO42-向c移动 |
| C、电池工作的过程中,d电极上产生大量的气泡 |
| D、电池工作的过程中,溶液中SO42-浓度基本不变 |
下列变化,需要加入适当的氧化剂才能完成的是( )
| A、PCl3→PCl5 |
| B、MnO4-→Mn2+ |
| C、SO2→SO32- |
| D、Cl2→HClO |
下列物质的分子中,属于正四面体结构的是( )
| A、CHCl3 |
| B、CH4 |
| C、CH2Cl2 |
| D、CH3Cl |
下列关于化学键的叙述,正确的一项是( )
| A、离子化合物中一定含有离子键 |
| B、单质分子中均不存在化学键 |
| C、离子化合物中一定不含共价键 |
| D、含有共价键的化合物一定是共价化合物 |