题目内容
已知:4NH3+5O2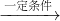 4NO+6H2O;4NO+3O2+2H2O→4HNO3
4NO+6H2O;4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空:
(1)amol NO完全转化为HNO3需要空气______mol;
(2)为使NH3恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为______(保留2位小数).
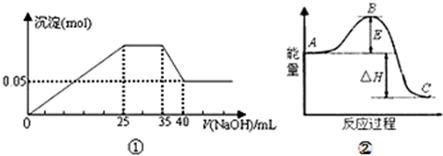
(3)20.0moL的NH3用空气氧化,产生混合物的组成为:NO 18.0mol、O2 12.0mol、N2 150.0mol和一定量的硝酸,以及其它成分.(高温下NO和O2不反应)计算氨转化为NO和HNO3的转化率.
解:(1)设需要空气的物质的量为x,
4NO+2H2O+3O2=4HNO3
4mol 3mol
amol 0.20x
x=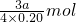 =3.75amol,
=3.75amol,
则需要空气的物质的量为3.75a mol,故答案为:3.75a;
(2)假设氨气的体积是4L,设需要空气的体积为y,
4NH3+5O2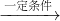 4NO+6H2O
4NO+6H2O
4 5
4L 0.20y
y=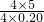 L=25L,
L=25L,
氨-空气混合物中氨的体积分数=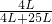 =0.14,
=0.14,
故答案为:0.14;
(3)设生成x mol HNO3,空气中氮气的量是氧气的 4倍,4(2x+18.0×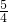 +12.0)=150.0 x=1.5(mol)
+12.0)=150.0 x=1.5(mol)
根据氮原子守恒,NH3的转化为HNO3的转化率=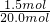 ×100%=7.5%
×100%=7.5%
NH3的转化为NO的转化率=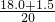 ×100%=97.5%,
×100%=97.5%,
答:氨转化为NO和HNO3的转化率分别是7.5%和97.5%.
分析:(1)根据一氧化氮和氧气的关系式计算;
(2)根据氨气计算需要氧气的量,再根据体积分数公式进行计算;
(3)根据反应过程中氮气的量不变进行计算,算出生成硝酸的物质的量,再根据原子守恒计算转化率.
点评:本题考查了氧化还原反应的计算,难点是计算转化率,明确氮气和氧气的关系是解本题的关键,结合原子守恒来分析解答,难度较大.
4NO+2H2O+3O2=4HNO3
4mol 3mol
amol 0.20x
x=
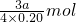 =3.75amol,
=3.75amol,则需要空气的物质的量为3.75a mol,故答案为:3.75a;
(2)假设氨气的体积是4L,设需要空气的体积为y,
4NH3+5O2
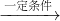 4NO+6H2O
4NO+6H2O4 5
4L 0.20y
y=
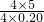 L=25L,
L=25L,氨-空气混合物中氨的体积分数=
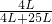 =0.14,
=0.14,故答案为:0.14;
(3)设生成x mol HNO3,空气中氮气的量是氧气的 4倍,4(2x+18.0×
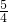 +12.0)=150.0 x=1.5(mol)
+12.0)=150.0 x=1.5(mol)根据氮原子守恒,NH3的转化为HNO3的转化率=
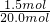 ×100%=7.5%
×100%=7.5% NH3的转化为NO的转化率=
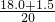 ×100%=97.5%,
×100%=97.5%,答:氨转化为NO和HNO3的转化率分别是7.5%和97.5%.
分析:(1)根据一氧化氮和氧气的关系式计算;
(2)根据氨气计算需要氧气的量,再根据体积分数公式进行计算;
(3)根据反应过程中氮气的量不变进行计算,算出生成硝酸的物质的量,再根据原子守恒计算转化率.
点评:本题考查了氧化还原反应的计算,难点是计算转化率,明确氮气和氧气的关系是解本题的关键,结合原子守恒来分析解答,难度较大.

练习册系列答案
相关题目
某100mL溶液中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各离子的物质的量均为0.1mol.
| 阴离子 | SO42-、NO3-、Cl- |
| 阳离子 | Fe3+、Fe2+、NH4+、Cu2+、Al3+ |
②若向原溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变.
③若向原溶液中加入BaCl2溶液,有白色沉淀生成.
试回答下列问题:
(1)原溶液中所含阳离子是(写离子符号,后同)______,阴离子是______;
(2)若向原溶液中先加入少量盐酸,再滴入KSCN溶液,实验中所发生反应的离子方程式是______,______;
(3)若向原溶液中加入足量NaOH溶液,充分反应后静置一段时间,过滤、洗涤、灼烧,最终所得固体的质量是______;
(4)向原溶液中加入足量盐酸后,用排水法收集所产生的气体并使气体恰好充满容器,仍将容器倒置于水槽中,再向容器中通入______ mL O2(气体体积均指标准状况),能使溶液充满该容器.
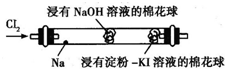 某化学教师为“氯气与金属钠的反应”设计了如图所示的装置(加热装置省略)来替代相关的教材实验装置.先给钠预热,当钠熔化成圆球时,撤火,通入氯气,即可观察到钠着火燃烧,并产生大量白烟.
某化学教师为“氯气与金属钠的反应”设计了如图所示的装置(加热装置省略)来替代相关的教材实验装置.先给钠预热,当钠熔化成圆球时,撤火,通入氯气,即可观察到钠着火燃烧,并产生大量白烟.