题目内容
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA个电子 |
| B、1 mol Al分别放入足量的冷的浓HNO3、稀HNO3中,反应后转移的电子均为3NA |
| C、各5.6 g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA |
| D、24 g镁与足量的盐酸或NaOH溶液反应转移的电子数目均为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.钠为1价金属,1mol钠完全反应失去1mol电子;
B.铝与冷的浓硝酸发生钝化现象,阻止了反应的继续进行;
C.铁与氯气反应生成氯化铁、铁与盐酸反应生成氯化亚铁;
D.镁与盐酸反应生成氯化镁和氢气,但是镁不与氢氧化钠溶液反应.
B.铝与冷的浓硝酸发生钝化现象,阻止了反应的继续进行;
C.铁与氯气反应生成氯化铁、铁与盐酸反应生成氯化亚铁;
D.镁与盐酸反应生成氯化镁和氢气,但是镁不与氢氧化钠溶液反应.
解答:
解:A.1mol钠完全反应,无论生成氧化钠还是过氧化钠,失去的电子都是1mol,失去NA个电子,故A正确;
B.1 molAl分别放入足量的冷的浓HNO3、稀HNO3中,铝与冷的浓硝酸发生钝化,无法计算转移的电子数,故B错误;
C.5.6g铁的物质的量为0.1mol,0.1mol铁与盐酸反应生成氯化亚铁,失去0.2mol电子,电子转移总数均为0.2NA,故C错误;
D.24g镁的物质的量为1mol,镁不与氢氧化钠溶液反应,故D错误;
故选A.
B.1 molAl分别放入足量的冷的浓HNO3、稀HNO3中,铝与冷的浓硝酸发生钝化,无法计算转移的电子数,故B错误;
C.5.6g铁的物质的量为0.1mol,0.1mol铁与盐酸反应生成氯化亚铁,失去0.2mol电子,电子转移总数均为0.2NA,故C错误;
D.24g镁的物质的量为1mol,镁不与氢氧化钠溶液反应,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确分子、原子、原子核内质子中子及核外电子的构成关系,选项C为易错点,注意常温下铁、铝与浓硫酸、浓硝酸发生钝化,试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
如图装置分别通电一段时间后,溶液的质量增加的是( )
A、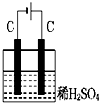 |
B、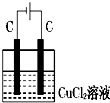 |
C、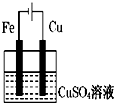 |
D、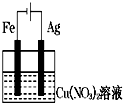 |
有a、b、c、d四种主族元素,已知a、b的阳离子和c、d的阴离子都具有相同的电子层结构,而且原子半径a>b,阴离子所带的负电荷数为c>d.则四种元素核电荷数由小到大的顺序为( )
| A、d<c<a<b |
| B、c<d<b<a |
| C、d<a<b<c |
| D、c<d<a<b |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、含有NA个氩原子的氩气在标准状况下的体积约为11.2 L |
| B、17g 氨气含有的电子数为10NA |
| C、18g D2O中含有的氧原子数为NA |
| D、标准状况下,22.4LCCl4含有的分子数为NA |
能正确表示下列反应的离子方程式是( )
| A、Ba(OH)2与稀H2SO4反应 Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B、饱和碳酸钠溶液中通入足量CO2 CO32-+H2O+CO2═2HCO3- |
| C、C12与NaOH溶液反应 Cl2+2OH-═C1-+C1O-+H2O |
| D、把金属铁放入稀硫酸中 2Fe+6H+═2Fe3++3H2↑ |