题目内容
11.如图所示,烧杯中都盛有稀硫酸.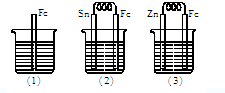
(1)中反应的离子方程式为Fe+2H+=Fe2++H2↑.
(2)中的电极反应:Fe:Fe-2e-=Fe2+Sn:2H++2e-=H2↑.
(3)中被腐蚀的金属是Zn其电极反应式为Zn-2e-=Zn2+.
分析 (1)中铁和稀硫酸发生置换反应;
(2)中铁易失电子作负极、Sn作正极,负极上铁失电子发生氧化反应、正极上氢离子放电;
(3)该装置中,锌易失电子作负极、Fe作正极,作负极的金属易被腐蚀.
解答 解:(1)中铁和稀硫酸发生置换反应生成亚铁离子和氢气,电极反应式为Fe+2H+=Fe2++H2↑,
故答案为:Fe+2H+=Fe2++H2↑;
(2)该装置中Fe易失电子作负极、Sn作正极,负极电极反应为Fe-2e=Fe2+、正极电极反应为2H++2e=H2↑,
故答案为:Fe-2e=Fe2+;2H++2e=H2↑;
(3)该装置中,锌易失电子作负极、Fe作正极,作原电池负极的金属易被腐蚀,所以被腐蚀的金属是Zn,电极反应为Zn-2e═Zn2+,
故答案为:Zn;Zn-2e═Zn2+.
点评 本题考查了原电池原理,根据失电子难易程度确定正负极,知道金属腐蚀快慢顺序,题目难度不大.

练习册系列答案
相关题目
2.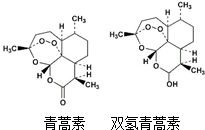 双氢青蒿素的抗疟疗效是青蒿素的10倍,其结构如图所示,下列说法中错误的是( )
双氢青蒿素的抗疟疗效是青蒿素的10倍,其结构如图所示,下列说法中错误的是( )
 双氢青蒿素的抗疟疗效是青蒿素的10倍,其结构如图所示,下列说法中错误的是( )
双氢青蒿素的抗疟疗效是青蒿素的10倍,其结构如图所示,下列说法中错误的是( )| A. | 双氢青蒿素的分子式为C15H22O5 | |
| B. | 由青蒿素制备双氢青蒿素的反应属还原反应 | |
| C. | 青蒿素分子中含有过氧链和酯基、醚键 | |
| D. | 双氢青蒿素分子中有2个六元环和2个七元环 |
19.有关化学用语正确的( )
| A. | 乙烯的结构式:C2H4 | B. | 甲烷分子的比例模型: | ||
| C. | 四氯化碳的电子式: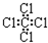 | D. | 苯的分子式: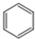 |
16.硬水经磺化煤(NaR)软化后,其水中阳离子浓度最大的是( )
| A. | Ca2+ | B. | Mg2+ | C. | Na+ | D. | H+ |
1.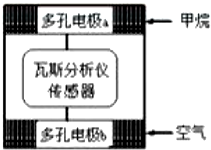 瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )
 瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )| A. | 瓦斯分析仪工作时,电池内电路中电子由电极b 流向电极a | |
| B. | 电极b 是正极,O2-由电极 a流向电极b | |
| C. | 电极a的反应式为:CH4+4O2--8e-=CO2+2H2O | |
| D. | 当固体电解质中有1 mol O2- 通过时,电子转移 4 mol |
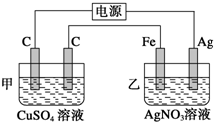 用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加.
用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加.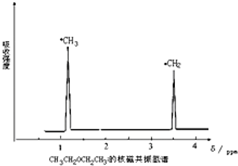 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.例如二乙醚的结构简式为:CH3-CH2-O-CH2-CH3,其核磁共振谱中给出的峰值(信号)有两个,如图所示:
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.例如二乙醚的结构简式为:CH3-CH2-O-CH2-CH3,其核磁共振谱中给出的峰值(信号)有两个,如图所示: