题目内容
1.下列叙述正确的是( )| A. | 构成原电池正极和负极的材料必须是两种活动性不同的金属 | |
| B. | 由CH4、O2和KOH构成的燃料电池中,通入CH4的电极为正极 | |
| C. | 原电池工作时,负极发生氧化反应,化合价降低 | |
| D. | 铜锌原电池工作时,当有13 g锌溶解时,电路中有0.4 mol电子通过 |
分析 A、正极和负极可以是两种不同的金属,也可以是导电的非金属与金属;
B、CH4发生氧化反应为负极;
C、原电池工作时,负极失电子,发生氧化反应,化合价升高;
D、铜锌原电池工作时,根据Zn和转移电子之间的关系式计算.
解答 解:A、正极和负极可以是两种不同的金属,也可以是导电的非金属(碳棒)与金属,故A错误;
B、CH4发生氧化反应为负极,而不是正极,故B错误;
C、原电池工作时,负极失电子,发生氧化反应,化合价升高,而不是降低,故C错误;
D、铜锌原电池工作时,若有13g锌被溶解,电路中电子转移的物质的量=$\frac{13g}{65g/mol}$=0.4mol,故D正确;
故选D.
点评 本题考查了原电池和电解池原理,知道原电池正负极的判断方法、各个物理量之间的关系、电极上发生的反应即可解答,易错选项是A,原电池电极可能是金属也可能不是金属,为易错点.

练习册系列答案
相关题目
12.已知:2Na[Al(OH)4]+CO2+3H2O=2Al(OH)3↓+Na2CO3.向含2mol NaOH、1mol Ba(OH)2、2mol Na[Al(OH)4]的混合溶液中慢慢通入CO2,则通入CO2的量和生成沉淀的量关系不正确的是( )
| 选项 | A | B | C | D |
| n(CO2)(mol) | 6 | 4 | 3 | 2 |
| n(沉淀)(mol) | 2 | 3 | 2 | 1 |
| A. | A | B. | B | C. | C | D. | D |
9.下列化学用语表示正确的是( )
| A. | 铁原子的电子排布式:[Ar]3d64s2 | B. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | ||
| C. | 氢氧化钠的电子式: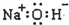 | D. | F的原子结构示意图: |
16.醋酸溶液中存在电离平衡:CH3COOH?H++CH3COO-下列叙述不正确的是( )
| A. | 醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) | |
| B. | CH3COOH溶液加醋酸钠溶液,因醋酸根水解显碱性,电离平衡向正反应方向移动 | |
| C. | CH3COOH溶液中加入少量的CH3COONa固体,平衡逆向移动 | |
| D. | 常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
10.${\;}_{\;}^{16}$O和${\;}_{\;}^{18}$O是氧元素的两种核素,设NA为阿伏加德罗常数值,下列说法正确的是( )
| A. | ${\;}_{\;}^{16}$O2与${\;}_{\;}^{18}$O2互为同位素 | |
| B. | 等质量的${\;}_{\;}^{16}$O2与${\;}_{\;}^{18}$O2所含有的分子数相同 | |
| C. | 标准状况下,1.12L${\;}_{\;}^{16}$O2和1.12L${\;}_{\;}^{18}$O2均含有0.1NA个氧原子 | |
| D. | 通过化学变化可以实现${\;}_{\;}^{16}$O2与${\;}_{\;}^{18}$O2间的相互转化 |

