题目内容
下列离子方程式中正确的是( )
| A、稀盐酸滴在石灰石上:CaCO3+2H+═Ca2++H2CO3 |
| B、硝酸银溶液与食盐水的反应:Ag++Cl-═AgCl↓ |
| C、锌与盐酸的反应:Zn+2H++2Cl-═Zn2++2Cl-+H2↑ |
| D、氧化铜与稀硫酸的反应:CuO+2H++SO42-═CuSO4+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸要写成二氧化碳和水;
B.氯化银是白色沉淀;
C.氯离子应该删掉;
D.硫酸铜不是沉淀,需要拆成离子.
B.氯化银是白色沉淀;
C.氯离子应该删掉;
D.硫酸铜不是沉淀,需要拆成离子.
解答:
解:A.稀盐酸滴在石灰石上离子方程式为:CaCO3+2H+═Ca2++CO2↑+H2O,故A错误;
B.硝酸银溶液与食盐水的反应:Ag++Cl-═AgCl↓,故B正确;
C.锌与盐酸的反应:Zn+2H+═Zn2++H2↑,故C错误;
D.氧化铜与稀硫酸的反应:CuO+2H+═Cu2++H2O,故错误;
故选B.
B.硝酸银溶液与食盐水的反应:Ag++Cl-═AgCl↓,故B正确;
C.锌与盐酸的反应:Zn+2H+═Zn2++H2↑,故C错误;
D.氧化铜与稀硫酸的反应:CuO+2H+═Cu2++H2O,故错误;
故选B.
点评:本题考查离子反应方程式的正误判断,明确发生的化学反应及离子反应的书写方法即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列推断正确的是( )
| A、Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 |
| B、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| C、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D、SiO2 是酸性氧化物,能与NaOH溶液反应 |
取三张蓝色石蕊试纸放在玻璃棒上,然后按顺序分别摘加69% HNO3,98.3% H2SO4和新 制氯水,三张试纸最后呈现的颜色依次为( )
| A、白 红 白 |
| B、红 黑 红 |
| C、红 红 红 |
| D、白 黑 白 |
X、Y、Z、M、W原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍,Z与其同主族的短周期无素可形成一种常见气体,X、Y、Z3种元素形成化合物甲,下列说法不正确的是( )
| A、原子半径:W>Y>Z>M>X |
| B、化合物甲中可能含有离子键和共价键 |
| C、由W元素形成的单质在自然界的贮量丰富,并存在大量的单质 |
| D、X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM |
已知X,Y声是元素周期表中前20号元素:|x-y|=3,X,Y能形成化合物M,下列说法正确的是( )
| A、若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B、若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C、若M属于共价化合物,则该分子中原子个数比可能为1:2 |
| D、若M属于离子化合物,则该化合物中只存在离子键 |
某同学用Na2CO3配制0.10mol/L Na2CO3溶液的过程如图所示.你认为该同学的错误有( )
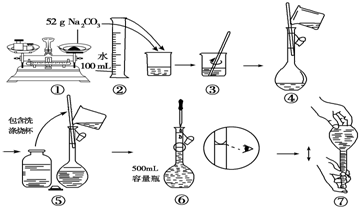

| A、①⑤⑥ | B、②④⑦ |
| C、①⑥ | D、⑤⑥⑦ |