题目内容
甲醛是世界卫生组织确认的致癌致畸物质之一.我国规定:室内甲醛含量不得超过8×10-5mg/L.某研究性学习小组利用酸性KMnO4溶液测定居室内空气中甲醛的含量.
[实验原理]
KMnO4(H+)溶液为强氧化剂,可氧化甲醛,反应方程式为:
4MnO4-+5HCHO+12H+═4Mn2++5CO2+11H2O
ab5.00mL1.00×10-3mol?L-1KMnO4(滴有几滴稀H2SO4)
[实验装置]
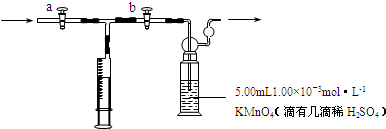
[实验步骤]
(1)先准确量取5.00mL 1.00×10-3mol?L-1KMnO4溶液于洗气瓶中,并滴入几滴稀H2SO4,加水20mL稀释备用.
(2)先打开 ,关闭 (填“a”或“b”),每次用注射器抽取100mL某新装修的房屋室内空气.后关闭 ,打开 (填“a”或“b”),再推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应,如此反复多次直至任务完成.
[交流讨论]
(1)某同学用该方法测量空气中甲醛的含量时,所测得的数值比实际含量低,你认为其可能的原因是(假设溶液配制、量取过程均无错误):
① ;
② .
(至少答出2种可能性)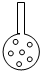
(2)实验结束后,该小组成员在相互交流的过程中认为:
①实验装置应加以改进.有同学提议:可将插入KMnO4溶液的管子下端改成具有多孔的球泡(如图),有利于提高实验的准确度,其理由是 .
②实验原理可以改进.
实验中直接抽取室内空气再压送到洗气瓶中至KMnO4溶液刚好褪色,抽气次数太多,太麻烦.有同学提议:通过测定洗气瓶中KMnO4的剩余量,可大大减少抽气的次数,也可达到实验目的,你认为是否可行: .(填“是”或“否”)
(3)若该研究性学习小组的同学共抽气500次并压送到洗气瓶中使KMnO4溶液的红色刚好褪去,则该居室内空气中甲醛的浓度为: mg/L.你认为该居室内空气中甲醛含量是否超过我国规定: .(填“是”或“否”)
[实验原理]
KMnO4(H+)溶液为强氧化剂,可氧化甲醛,反应方程式为:
4MnO4-+5HCHO+12H+═4Mn2++5CO2+11H2O
ab5.00mL1.00×10-3mol?L-1KMnO4(滴有几滴稀H2SO4)
[实验装置]

[实验步骤]
(1)先准确量取5.00mL 1.00×10-3mol?L-1KMnO4溶液于洗气瓶中,并滴入几滴稀H2SO4,加水20mL稀释备用.
(2)先打开
[交流讨论]
(1)某同学用该方法测量空气中甲醛的含量时,所测得的数值比实际含量低,你认为其可能的原因是(假设溶液配制、量取过程均无错误):
①
②
(至少答出2种可能性)

(2)实验结束后,该小组成员在相互交流的过程中认为:
①实验装置应加以改进.有同学提议:可将插入KMnO4溶液的管子下端改成具有多孔的球泡(如图),有利于提高实验的准确度,其理由是
②实验原理可以改进.
实验中直接抽取室内空气再压送到洗气瓶中至KMnO4溶液刚好褪色,抽气次数太多,太麻烦.有同学提议:通过测定洗气瓶中KMnO4的剩余量,可大大减少抽气的次数,也可达到实验目的,你认为是否可行:
(3)若该研究性学习小组的同学共抽气500次并压送到洗气瓶中使KMnO4溶液的红色刚好褪去,则该居室内空气中甲醛的浓度为:
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:[实验步骤]
(2)打开a关闭b收集室内空气,然后关闭a打开b将橡皮囊中的气体压缩到酸性高锰酸钾溶液中;
[交流讨论]
(1)从实验各个环节可能出现的问题分析;
(2)①根据反应物的接触面积越大,反应越充分来回答;
②通过测定洗气瓶中KMnO4的剩余量,可以得到参加反应的高锰酸钾的量,根据反应可以计算甲醛的量;
(3)根据恰好反应进行完,酸性KMnO4溶液颜色褪去;根据化学方程式4MnO4-+5HCHO+12H+=4Mn2++5CO2↑+11H2O求出HCHO的物质的量,然后求出其体积,最后求出甲醛的浓度.
(2)打开a关闭b收集室内空气,然后关闭a打开b将橡皮囊中的气体压缩到酸性高锰酸钾溶液中;
[交流讨论]
(1)从实验各个环节可能出现的问题分析;
(2)①根据反应物的接触面积越大,反应越充分来回答;
②通过测定洗气瓶中KMnO4的剩余量,可以得到参加反应的高锰酸钾的量,根据反应可以计算甲醛的量;
(3)根据恰好反应进行完,酸性KMnO4溶液颜色褪去;根据化学方程式4MnO4-+5HCHO+12H+=4Mn2++5CO2↑+11H2O求出HCHO的物质的量,然后求出其体积,最后求出甲醛的浓度.
解答:
解:【实验步骤】打开a关闭b收集室内空气,然后关闭a打开b将橡皮囊中的气体压缩到酸性高锰酸钾溶液中,
故答案为:酸式滴定管(或移液管) a、b,a、b;
【交流讨论】
(1)从实验各个环节可能出现的问题分析,如:未把橡皮囊中气体完全压出、压送气体速度过快、装置气密性较差、导气管伸入KMnO4溶液中太浅、同一地点取样次数太多等,
故答案为:注射器压送气体速度过快、装置气密性较差;导气管伸入KMnO4溶液中太浅、同一地点取样次数太多;
(2)①将插入KMnO4溶液的管子下端改成具有多孔的球泡,反应物的接触面积越大,反应越充分,则测量越准确,有利于提高实验的准确度.
故答案为:可增大气体与溶液的接触面积,使空气中的HCHO被充分吸收;
②通过测定洗气瓶中KMnO4的剩余量,可以得到参加反应的高锰酸钾的量,根据反应可以计算甲醛的量,这样可大大减少抽气的次数,也可达到实验目的,故答案为:是;
(3)抽气500次,则会抽到空气体积是100mL×500=50000mL=50L,根据反应,设:抽得的气体中含有甲醛的物质的量是n,则
4MnO4-+5HCHO+12H+═4Mn2++5CO2+11H2O,
4 5
0.005L×1.00×10-3mol?L-1 n
解得n=
=6.25×10-6mol,质量是6.25×10-6mol×30g/mol=1.875×
10-4g,该居室内空气中甲醛的浓度为
=3.75×10-3mg/L,该居室内空气中甲醛含量超过我国规定,故答案为:3.75×10-3mg/L;是.
故答案为:酸式滴定管(或移液管) a、b,a、b;
【交流讨论】
(1)从实验各个环节可能出现的问题分析,如:未把橡皮囊中气体完全压出、压送气体速度过快、装置气密性较差、导气管伸入KMnO4溶液中太浅、同一地点取样次数太多等,
故答案为:注射器压送气体速度过快、装置气密性较差;导气管伸入KMnO4溶液中太浅、同一地点取样次数太多;
(2)①将插入KMnO4溶液的管子下端改成具有多孔的球泡,反应物的接触面积越大,反应越充分,则测量越准确,有利于提高实验的准确度.
故答案为:可增大气体与溶液的接触面积,使空气中的HCHO被充分吸收;
②通过测定洗气瓶中KMnO4的剩余量,可以得到参加反应的高锰酸钾的量,根据反应可以计算甲醛的量,这样可大大减少抽气的次数,也可达到实验目的,故答案为:是;
(3)抽气500次,则会抽到空气体积是100mL×500=50000mL=50L,根据反应,设:抽得的气体中含有甲醛的物质的量是n,则
4MnO4-+5HCHO+12H+═4Mn2++5CO2+11H2O,
4 5
0.005L×1.00×10-3mol?L-1 n
解得n=
| 5×0.005L×1.00×10-3mol/L |
| 4 |
10-4g,该居室内空气中甲醛的浓度为
| 1.875×10-4×103mg |
| 50L |
点评:本题主要考查了甲醛的性质、含量的测定原理等知识,难度大,知识点较多.

练习册系列答案
相关题目
下列物质的使用不涉及化学变化的是( )
| A、用活性炭去除冰箱中的异味 |
| B、用热碱水清除炊具上残留的油污 |
| C、用浸泡过高锰酸钾溶液的硅藻土保鲜水果 |
| D、用含硅胶、铁粉的透气小袋与食品一起密封包装 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1molCl2参加的任何反应,反应过程中转移电子数都是2NA | ||
| B、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | ||
C、标准状况下,1L乙醇完全燃烧产生CO2分子的数目为
| ||
| D、将10mL质量分数为98%的浓H2SO4,用水稀释至100mL,H2SO4的质量分数大于9.8% |
 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: 某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如图所示的实验装置.请你根据他们的思路,完成下述的实验报告.
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如图所示的实验装置.请你根据他们的思路,完成下述的实验报告.