题目内容
18.化学与生活息息相关,下列说法不正确的是( )| A. | 建筑要使用大量的沙,常使用内陆河的河沙及海洋的海沙 | |
| B. | 含次氯酸盐的漂白粉与含盐酸的洁厕灵混合使用会产生有毒气体 | |
| C. | 漂白粉和明矾都常用于自来水的处理,二者的作用和原理不相同 | |
| D. | 绿色化学的核心是从源头上减少和消除化工生产对环境的污染 |
分析 A.不能使用海沙做建筑材料,防止钢铁发生腐蚀;
B.依据次氯酸根离子与氯离子酸性环境下发生归中反应生成氯气解答;
C.漂白粉生成具有强氧化性的次氯酸,明矾水解生成具有吸附性的氢氧化铝;
D.根据绿色化学的核心的概念.
解答 解:A.因为海沙盐分高,极易使建筑工程出现氯离子腐蚀钢筋情况,造成安全隐患,故A错误;
B.次氯酸根离子与氯离子酸性环境下发生归中反应生成氯气,氯气有毒,故B正确;
C.漂白粉生成具有强氧化性的次氯酸,能消毒杀菌,明矾水解生成具有吸附性的氢氧化铝,能起到吸附悬浮杂质的作用,做净水剂,二者原理不同,故C正确;
D.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染,故D正确;
故选:A.
点评 本题考查较为综合,综合考查元素化合物知识,侧重于化学与生活、生产、环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
8.如表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题.
(1)单质化学性质最不活泼的是Ne;
(2)地壳中含量最多的元素是氧(填名称);
(3)单质常用作半导体材料的是Si;
(4)Mg原子结构示意图为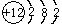 ;
;
(5)O和S中,原子半径较大的是S;
(6)CH4和NH3中,热稳定性较强的是NH3(或氨气);
(7)新制氯水有漂白作用,是因为其中含有HClO(填“HCl”或“HCIO”);
(8)元素最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式),两性氢氧化物是 Al(OH)3(填化学式);
(9)某烃分子中含有6个碳原子,结构简式为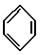 ,常用作有机溶剂.该有机物分子式为 C6H6 ,其中碳元素与氢元素的质量比m(C):m(H)=12:1(相对原子质量:H-1 C-12)
,常用作有机溶剂.该有机物分子式为 C6H6 ,其中碳元素与氢元素的质量比m(C):m(H)=12:1(相对原子质量:H-1 C-12)
| 族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)地壳中含量最多的元素是氧(填名称);
(3)单质常用作半导体材料的是Si;
(4)Mg原子结构示意图为
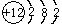 ;
;(5)O和S中,原子半径较大的是S;
(6)CH4和NH3中,热稳定性较强的是NH3(或氨气);
(7)新制氯水有漂白作用,是因为其中含有HClO(填“HCl”或“HCIO”);
(8)元素最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式),两性氢氧化物是 Al(OH)3(填化学式);
(9)某烃分子中含有6个碳原子,结构简式为
 ,常用作有机溶剂.该有机物分子式为 C6H6 ,其中碳元素与氢元素的质量比m(C):m(H)=12:1(相对原子质量:H-1 C-12)
,常用作有机溶剂.该有机物分子式为 C6H6 ,其中碳元素与氢元素的质量比m(C):m(H)=12:1(相对原子质量:H-1 C-12)
6.在含有大量的Na+、H+、NO3-的溶液中,还可能大量存在的离子是( )
| A. | Fe2+ | B. | HCO3- | C. | OH- | D. | NH4+ |
3.下列关于离子共存或离子反应的说法正确的是( )
| A. | 某无色溶液中可能大量存在:H+、Cl-、MnO${\;}_{4}^{-}$ | |
| B. | 室温下由水电离的 c(OH-)=1×10-12mol•L-1的溶液中能大量共存:K+、Na+、Cl-、HCO3- | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2 Fe3++2 Br2+6 Cl- | |
| D. | 稀硫酸和Ba(OH)2溶液反应:H++SO${\;}_{4}^{2-}$+Ba2++OH-═BaSO4↓+H2O |
10.下列说法中正确的是( )
| A. | 盐中一定含有金属元素 | B. | 氢化物一定是共价化合物 | ||
| C. | 碱中一定含有氢、氧元素 | D. | 能电离出H+的物质一定是酸 |
7.现将6.96g 的MnO2与100g 35.6%的盐酸(盐酸足量)共热,向反应后的溶液中加水稀释到250mL,取25mL跟足量的AgNO3溶液反应.若不考虑HCl的挥发,下列说法正确的是( )
| A. | 产生氯气1.792L | B. | 生成AgCl沉淀11.7g | ||
| C. | 被还原的HCl为0.16mol | D. | 转移的电子数为0.16个 |
8.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向某无色溶液中滴加氯水后,再滴加淀粉溶液 | 溶液变为蓝色 | 原溶液为KI溶液 |
| B | 向10mL浓度均为0.1mol/L的MgCl2和CuCl2的混合溶液中滴加一滴0.1mol/L的NaOH溶液 | 出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| C | 向某未知溶液中滴加稀盐酸后产生无色气体,气体通入品红溶液中 | 品红溶液褪色 | 原溶液中有SO32- |
| D | 用刚洗净未干燥的容量瓶配制0.1mol/L的NaOH溶液 | 所配制的溶液浓度偏小 |
| A. | A | B. | B | C. | C | D. | D |
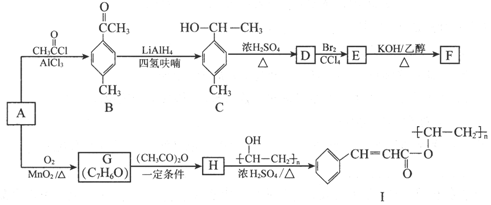
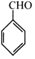
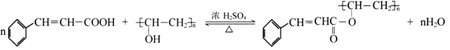
 (写出其中一种的结构简式).
(写出其中一种的结构简式).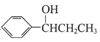 的合成路线
的合成路线 .
.