题目内容
根据中学化学课本中的数据资料作出以下推断,其中不正确的是( )
| A、利用化合价数据可以确定某些元素原子的最外层电子数 |
| B、利用密度数据可判断液体物质挥发性的大小 |
| C、利用溶解度数据可推测将一些物质混合物分离开来的可能性 |
| D、利用原子半径数据可推断某些原子的氧化性和还原性的强弱 |
考点:原子结构与元素的性质,氧化性、还原性强弱的比较,物质的分离、提纯和除杂
专题:基本概念与基本理论
分析:A.主族元素中元素最高正化合价与其最外层电子数相等,但O、F元素除外;
B.液体挥发性大小与其密度无关;
C.可以利用物质溶解度不同将混合物分离开;
D.同一周期元素,原子半径随着原子序数增大而减小,其氧化性随着原子序数增大而增强;同一主族元素,原子半径随着原子序数增大而增大,同一主族元素单质,其氧化性随着原子序数增大而减弱,其还原性随着原子序数增大而减小.
B.液体挥发性大小与其密度无关;
C.可以利用物质溶解度不同将混合物分离开;
D.同一周期元素,原子半径随着原子序数增大而减小,其氧化性随着原子序数增大而增强;同一主族元素,原子半径随着原子序数增大而增大,同一主族元素单质,其氧化性随着原子序数增大而减弱,其还原性随着原子序数增大而减小.
解答:
解:A.主族元素中元素最高正化合价与其最外层电子数相等,但O、F元素除外,所以利用化合价数据可以确定某些元素原子的最外层电子数,如Na、Mg等,故A正确;
B.酒精的密度比水小,酒精比水容易挥发,浓硫酸的密度比水大,浓硫酸比水更不容易挥发,所以物质的密度和液体物质挥发性的大小没有必然的联系,故B错误;
C.可以利用物质溶解度不同将混合物分离开,如根据碳酸钙和氯化钠的溶解度,采用溶解、过滤的方法将两种物质分离,故C正确;
D.利用原子半径数据可推断某些原子的氧化性和还原性的强弱,如第IA族元素单质,元素的原子半径越大,其失电子能力越强,其单质的还原性越强,故D正确;
故选B.
B.酒精的密度比水小,酒精比水容易挥发,浓硫酸的密度比水大,浓硫酸比水更不容易挥发,所以物质的密度和液体物质挥发性的大小没有必然的联系,故B错误;
C.可以利用物质溶解度不同将混合物分离开,如根据碳酸钙和氯化钠的溶解度,采用溶解、过滤的方法将两种物质分离,故C正确;
D.利用原子半径数据可推断某些原子的氧化性和还原性的强弱,如第IA族元素单质,元素的原子半径越大,其失电子能力越强,其单质的还原性越强,故D正确;
故选B.
点评:本题考查对教材中数据资料的分析,同时考查学生对教材知识的理解及应用能力,在分析问题时要结合其条件限制,排除一些特殊现象,题目难度中等.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
下列各组溶液,同时开始反应,出现浑浊最早的是( )
| A、20℃时5mL 0.05mol?L-1 Na2S2O3溶液与5mL 0.1mol?L-1硫酸混合 |
| B、20℃时 50mL0.1mol/L Na2S2O3溶液与50mL 0.1mol?L-1硫酸混合 |
| C、10℃时5mL 0.05mol?L-1 Na2S2O3溶液与5mL 0.1mol?L-1硫酸混合 |
| D、10℃时 5mL 0.1mol?L-1 Na2S2O3溶液与5mL 0.1mol?L-1硫酸混合 |
有化学方程式为:①SiO2+2C
Si+2CO ②Si+2Cl2
SiCl4 ③SiCl4+2H2Si+4HCl,其中,反应①和③属于( )
| ||
| ||
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |
下列有关碱金属元素的性质判断正确的是( )
| A、K与水反应最剧烈 |
| B、Rb比Na活泼,故Rb可以从Na的盐溶液中置换出Na |
| C、碱金属的阳离子没有还原性,所以有强氧化性 |
| D、从Li到Cs都易失去最外层一个电子,且失电子能力逐渐增强 |
根据如图信息判断,下列叙述正确的是( )


| A、硝酸钾的溶解度随温度升高而减小 |
| B、t2℃时,100g饱和硝酸钾溶液中溶有硝酸钾85g |
| C、t1℃时,氯化钠和硝酸钾的溶解度相同 |
| D、将t1℃时的硝酸钾饱和溶液升温到t2℃,有晶体析出 |
 阿司匹林是常见的解热镇痛药,结构简式如图所示,有关阿司匹林的说法正确的是( )
阿司匹林是常见的解热镇痛药,结构简式如图所示,有关阿司匹林的说法正确的是( )| A、能发生取代、酯化反应,但不能发生氧化、还原反应 |
| B、阿司匹林分子中最多可以有13个原子在同一平面上 |
| C、1mol该物质完全氧化最多可消耗10mol氧气 |
| D、1mol该物质最多可与3mol NaOH发生反应 |
已知通过乙醇制取氢气有如下两条路线:则下列说法不正确的是( )
a.CH3CH2OH(g)+H2O(g)═4H2(g)+2CO(g)△H=+255.6kJ?mol-1
b.CH3CH2OH(g)+1/2O2(g)═3H2(g)+2CO(g)△H=+13.8kJ?mol-1.
a.CH3CH2OH(g)+H2O(g)═4H2(g)+2CO(g)△H=+255.6kJ?mol-1
b.CH3CH2OH(g)+1/2O2(g)═3H2(g)+2CO(g)△H=+13.8kJ?mol-1.
| A、由a、b知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ?mol-1 |
| B、从能量消耗的角度来看,b路线制氢更加有利 |
| C、乙醇可通过淀粉等生物原料发酵制得,属于可再生资源 |
| D、降低温度,可提高b路线中乙醇的转化率 |
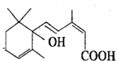 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,回答:
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,回答: