题目内容
已知NO2与N2O4相互转化:2NO2(g) N2O4(g);△H=-24.4kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的量浓度随时间变化的关系如下图。下列推理分析合理的是( )
N2O4(g);△H=-24.4kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的量浓度随时间变化的关系如下图。下列推理分析合理的是( )
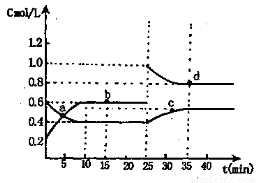
A.前10min内,用v(NO2)表示的该反应速率为0.02mol/(L·min)
B.反应进行到10min时,体系吸收的热量为9.76kJ
C.a,b,c,d四点中v正与v逆均相等
D.25min时,导致平衡移动的原因是升温
B
【解析】
试题分析:A、由图可知相同时间内,b物质的浓度变化是a物质浓度变化的2倍,所以b是二氧化氮,a是四氧化二氮,前10min内,用v(NO2)表示的该反应速率为(0.6-0.2)mol/L/10min=0.04mol/(L·min),错误;B、该反应是N2O4(g) 2NO2(g)△H=+24.4kJ/mol,反应进行到10min时,消耗的四氧化二氮的物质的量是(0.6-0.4)mol/L×2L=0.4mol,所以体系吸收的热量是24.4kJ/mol×0.4mol=9.76kJ,正确; C、a点时反应未达平衡,所以v正>v逆,c点时v正<v逆,只有b、d两点表示平衡状态,正逆反应速率相等,错误;D、25min时,四氧化二氮的速率为改变,而二氧化氮的速率增大,所以导致平衡逆向移动的原因是增大二氧化氮的浓度,不是升温,错误,答案选B。
2NO2(g)△H=+24.4kJ/mol,反应进行到10min时,消耗的四氧化二氮的物质的量是(0.6-0.4)mol/L×2L=0.4mol,所以体系吸收的热量是24.4kJ/mol×0.4mol=9.76kJ,正确; C、a点时反应未达平衡,所以v正>v逆,c点时v正<v逆,只有b、d两点表示平衡状态,正逆反应速率相等,错误;D、25min时,四氧化二氮的速率为改变,而二氧化氮的速率增大,所以导致平衡逆向移动的原因是增大二氧化氮的浓度,不是升温,错误,答案选B。
考点:考查对化学平衡图像的分析及平衡移动原理的应用

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目

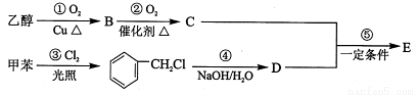
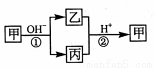
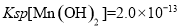 。工业上,调节pH沉淀废水中Mn2+.当pH=10时,溶液中c(Mn2?)= 。
。工业上,调节pH沉淀废水中Mn2+.当pH=10时,溶液中c(Mn2?)= 。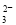 的水解程度和溶液的pH均增大
的水解程度和溶液的pH均增大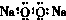
 Br
Br