题目内容
某学生用一定物质的量浓度的稀硫酸和氧化铜进行反应,实验结果如下由表数据可知稀硫酸和氧化铜恰好完全反应的是第( )次实验.
| 实验次数 | m(CuO)/(g) | 硫酸溶液/(ml) | m(CuSO4)/(g) |
| ① | 2.0 | 120 | 4.0 |
| ② | 4.0 | 120 | 8.0 |
| ③ | 6.0 | 120 | 9.6 |
| ④ | 8.0 | 200 | 16.0 |
| A、① | B、② | C、③ | D、④ |
考点:化学方程式的有关计算
专题:计算题
分析:根据表中提供的数据可以进行分析、判断,从而发现物质的变化规律,由1可知2.0g氧化铜可生成硫酸铜4g,所以可判断氧化铜的过量情况,酸有剩余即氧化铜完全反应后酸还有剩余的过程,利用表中的数据分析可完成相关的判断.
解答:
解:由①②③次实验可知,每2g氧化铜完全反应会生成4g硫酸铜,而由②到④的实验硫酸铜的量增加的不成比例,也就是当酸足量时6g氧化铜可生成12g硫酸铜,但却生成了9.6g说明酸量不足,又因为由4g氧化铜变到6g氧化铜时,硫酸铜的量有所增加,所以120mL的硫酸在①②步中一定会有剩余,所以3中氧化铜过量,则硫酸已全部反应,因此120mL硫酸最多生成硫酸铜的质量是9.6g硫酸铜,列比例式可求出200mL硫酸生成的硫酸铜的最大量是16,由④中可知生成16g硫酸铜需要氧化铜是8g,此时,稀硫酸和氧化铜恰好完全反应,
故选D.
故选D.
点评:该题是对数据分析知识的考查,解题的关键是找到数据中反应的相关规律,是一道训练学生思维能力的综合知识考查题.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
下列说法中,正确的是( )
| A、铅笔芯的主要成分是金属铅,儿童在使用是不可用嘴吮吸,以免引起铅中毒 |
| B、CO有毒,在生有炉火的居室中多放几盆水,可吸收CO,防止煤气中毒 |
| C、含氟冰箱产生的氟利昂是造成臭氧空洞的主要原因 |
| D、油条制作中常加入明矾作膨化剂,有利于补充身体所需微量元素,是理想早餐 |
下列实验操作中,主要不是从安全因素考虑的是( )
| A、点燃氢气前一定要检验氢气的纯度 |
| B、未使用完的白磷要随时收集起来,并与空气隔绝 |
| C、用氢气还原氧化铜时,要先通一会儿氢气,再加热氧化铜 |
| D、酒精灯不用时,必须盖上灯帽 |
下列物质的水溶液由于水解而呈碱性的是( )
| A、NaHSO4 |
| B、NaCl |
| C、Na2CO3 |
| D、NH3 |
下列说法正确的是( )
| A、某烷烃的名称为2,2,4,4-四甲基-3,3,5-三乙基己烷 |
B、化合物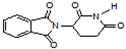 在酸性条件下水解,所得溶液加碱后加热有NH3生成 在酸性条件下水解,所得溶液加碱后加热有NH3生成 |
C、 可由其单体通过缩聚反应生成 可由其单体通过缩聚反应生成 |
| D、等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量不相等 |
下列固体混合物与过量的稀H2SO4反应,能产生气泡并有沉淀生产的是( )
| A、NaHCO3和Al(OH)3 |
| B、BaCl2和NaCl |
| C、KClO3和K2SO4 |
| D、Na2SO3和BaCO3 |
现有一块金属钠露置于空气中一段时间,为检验该固体是否部分变质为碳酸钠,先将固体样品溶解于水得到溶液,并采取下列措施,可以实现实验目的是( )
| A、测所得溶液的pH |
| B、取溶液滴入酚酞观察是否变红 |
| C、取溶液加入盐酸观察是否有气泡 |
| D、取溶液加入CuSO4观察是否有沉淀 |
