题目内容
6.某温度(t℃)时,水的Kw=10-13,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4的溶液bL混合,则:①若所得混合液为中性,则a:b=10:1;
②若所得混合液的pH=2,则a:b=9:2.
分析 某温度下Kw=10-13,此温度下pH=11的NaOH溶液,c(OH-)=$\frac{1{0}^{-13}}{1{0}^{-11}}$mol/L=0.01mol/L,pH=1的H2SO4溶液c(H+)=0.1mol/L,
(1)若所得混合液为中性,酸碱恰好完全反应;
(2)若所得混合液的pH=2,酸过量,根据c(H+)=$\frac{n({H}^{+})-n(O{H}^{-})}{V总}$计算.
解答 解:此温度下Kw=10-13,pH=11的NaOH溶液,c(OH-)=$\frac{1{0}^{-13}}{1{0}^{-11}}$mol/L=0.01mol/L,pH=1的H2SO4溶液c(H+)=0.1mol/L,则
(1)若所得混合液为中性,酸碱恰好完全反应,则有0.01mol/L×aL=0.1mol/L×bL,a:b=0.1:0.01=10:1,
故答案为:10:1;
(2)若所得混合液的pH=2,酸过量,c(H+)=$\frac{n({H}^{+})-n(O{H}^{-})}{V总}$=$\frac{0.1mol/L×bL-0.01mol/L×aL}{(a+b)L}$=0.01,
解之得:a:b=9:2,
故答案为:9:2.
点评 本题考查酸碱混合的计算,题目难度中等,解答本题的关键是把握当Kw=10-13时,溶液中c(OH-)、c(H+)的计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.已知:HNO2有氧化性,遇强氧化剂显还原性.某溶液中可能含有大量CO32-、S2-、SO32-、SO42-、NO3-、NO2-、OH-等阴离子.为检测上述阴离子,某研究性小组设计了下列实验:
①取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,将所得的气体依次通入品红溶液、足量酸性KMnO4溶液和澄清石灰水,品红褪色,石灰水变浑浊
②另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生
③另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色
④另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生
下列说法正确的是( )
①取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,将所得的气体依次通入品红溶液、足量酸性KMnO4溶液和澄清石灰水,品红褪色,石灰水变浑浊
②另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生
③另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色
④另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生
下列说法正确的是( )
| A. | 由①可推测溶液中一定含大量CO32-、S2-、SO32-、NO3- | |
| B. | 由②可推测溶液中一定含大量NO2- | |
| C. | 由③可推测溶液中一定含大量NO3- | |
| D. | 由实验④难以推测溶液中一定含大量SO42- |
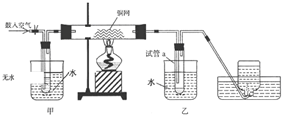
1.合成氨原料可以由天然气制取,其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1m3(标准状况)CH4按上式完全反应,产生H2134mol.
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应.1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为3<V<4.
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
该富氧空气中O2和N2的体积比V(O2)/V(N2)=$\frac{2}{3}$.
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,$\frac{V(H_{2})}{V(N_{2})}$=3:1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为(3-7a):3.
(1)1m3(标准状况)CH4按上式完全反应,产生H2134mol.
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应.1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为3<V<4.
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
| 气体 | CO | H2 | N2 | O2 |
| 体积(L) | 25 | 60 | 15 | 2.5 |
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,$\frac{V(H_{2})}{V(N_{2})}$=3:1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为(3-7a):3.
16.下列溶液中有关粒子的物质的量浓度关系正确的是( )
| A. | 氯水中:2c(Cl2)═c(ClO-)+c(Cl-)+c(HClO) | |
| B. | 25℃时,pH=12的NaOH溶液与pH=12的氨水;c(Na+)═c(NH4+) | |
| C. | pH=4的0.1 mol•L-1的NaHA溶液中:c(HA-)>c(H+)>c(H2A)>c(A2-) | |
| D. | 在K2CO3溶液中:c(CO32-)+c(H+)═c(HCO3-) |





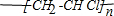
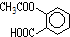 ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.