题目内容
4.如图是常见的两种实验操作,请回答下列问题: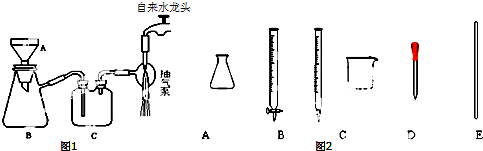
(1)减压过滤:
①写出图1中A、B两种仪器的名称:A布氏漏斗;B吸滤瓶;
②该装置图1有几处错误,请指出错误.布氏漏斗颈口斜面应与吸滤瓶的支管口相对;安全瓶的长管和短管连接顺序错误( 写出两处即可).
(2)用已知浓度的酸性高锰酸钾溶液滴定未知浓度的硫酸亚铁溶液:
①滴定终点的现象为加入最后一滴KMnO4溶液紫红色不褪,且半分钟内不褪色,滴定原理为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O(用离子反应方程式表示);
②滴定过程中可能用到如图2哪些仪器?AB.
分析 (1)减压的操作优点是:可加快过滤速度,并能得到较干燥的沉淀,所用仪器为布氏漏斗、吸滤瓶、安全瓶、抽气泵,使用时布氏漏斗颈口斜面应与吸滤瓶的支管口相对,且安全瓶中的导气管是短进长出;
(2)高锰酸钾本身有颜色,滴定亚铁离子不需要指示剂,当滴加最后一滴溶液后,溶液变成紫红色,30S内不褪色,说明达到滴定终点;亚铁离子具有还原性,高锰酸根离子具有氧化性,两者发生氧化还原反应;根据滴定操作方法选择使用的仪器.
解答 解:(1)①减压过滤所用仪器为A为布氏漏斗、B为吸滤瓶、C为安全瓶、抽气泵,
故答案为:布氏漏斗;吸滤瓶;
②根据减压过滤装置特点:布氏漏斗颈的斜口要远离且面向吸滤瓶的抽气嘴,并且安全瓶中的导气管是短进长出,所以图中错误为:布氏漏斗颈口斜面应与吸滤瓶的支管口相对;安全瓶的长管和短管连接顺序错误,
故答案为:布氏漏斗颈口斜面应与吸滤瓶的支管口相对;安全瓶的长管和短管连接顺序错误.
(2)①高锰酸钾本身有颜色,滴定亚铁离子不需要指示剂,当滴加最后一滴溶液后,溶液变成紫红色,30S内不褪色,说明达到滴定终点,亚铁离子具有还原性,高锰酸根离子具有氧化性,两者反应为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,
故答案为:加入最后一滴KMnO4溶液紫红色不褪,且半分钟内不褪色;5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
②滴定操作中需要使用滴定管和锥形瓶,即B、A正确,
故答案为:AB.
点评 本题考查学生常见的化学仪器,要求学生熟悉常见仪器,并掌握其应用,注意掌握过滤、滴定原理是解答本题的关键,题目难度不大.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目
15.下列说法不正确的是( )
| A. | 有些活泼金属如钠、镁、铝可作热还原法的还原剂 | |
| B. | 用电解熔融NaCl的方法来冶炼金属钠 | |
| C. | 回收废旧金属可以重新制成金属或它们的化合物 | |
| D. | 可用焦炭或一氧化碳还原氧化铝的方法来冶炼铝 |
12.某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.
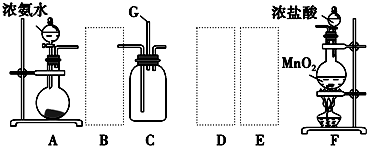
请回答下列问题:
(1)装置F中发生反应的离子方程式:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O.
(2)装置A中的烧瓶内固体可选用ABE(选填以下选项的代号).
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:
BⅠ,DⅡ,EⅢ.(均填编号)
(4)从装置C的出气管口处逸出的尾气可能含有污染环境的有毒气体,如何处理?氢氧化钠溶液吸收.原理是(用化学方程式表示):Cl2+2NaOH=NaCl+NaClO+H2O.

| Ⅰ | Ⅱ | Ⅲ | |
| 备选装置 |  | 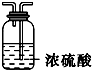 | 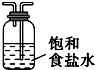 |
(1)装置F中发生反应的离子方程式:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O.
(2)装置A中的烧瓶内固体可选用ABE(选填以下选项的代号).
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:
BⅠ,DⅡ,EⅢ.(均填编号)
(4)从装置C的出气管口处逸出的尾气可能含有污染环境的有毒气体,如何处理?氢氧化钠溶液吸收.原理是(用化学方程式表示):Cl2+2NaOH=NaCl+NaClO+H2O.
19.合成氨工业对国民经济和社会发展具有重要的意义.哈伯法合成氨需要在20-50MPa的高压和500℃的高温下,并用铁作为催化剂,氨的转化率为10%-15%.最近美国俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)2的催化剂,在常温下合成出氨,反应方程式可表示为N2+3H2→2NH3,有关说法正确的是( )
| A. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 | |
| B. | 新法合成和哈伯法相比不需要在高温条件下,可节约大量能源,具有发展前景 | |
| C. | 新法合成能在常温下进行是因为不需要断裂化学键 | |
| D. | 新的催化剂升高了反应所需要的能量,提高了活化分子百分数 |
9.下列各选项中所述的两个量,前者一定大于后者的是 (各项所处温度都是相同的)( )
| A. | 稀盐酸与稀醋酸的导电性 | |
| B. | 物质的量浓度相等的 (NH4)2Fe(SO4)2溶液和 (NH4)2SO4溶液中NH4+的浓度 | |
| C. | 用量筒量取液体时,仰视的读数和俯视的读数 | |
| D. | 物质的量浓度相等的NaHCO3溶液和Na2CO3溶液中水的电离程度 |
13.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
| A. | 放电时负极反应式为:Zn-2e-+2OH-=Zn(OH)2 | |
| B. | 放电时每转移3mol电子,正极有1 mol K2FeO4被还原 | |
| C. | 充电时阴极附近溶液的碱性增强 | |
| D. | 放电时正极反应式为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
10.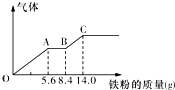 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A. | H2SO4浓度为2.5 mol•L-1 | |
| B. | OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 | |
| C. | 第二份溶液中最终溶质为FeSO4 | |
| D. | 原混合酸中NO3-物质的量为0.1 mol |