题目内容
2.在某温度下,可逆反应mA+nB?pC+qD的平衡常数为K,下列说法正确的是( )| A. | K随压强的改变而改变 | B. | K越大,C的平衡浓度越小 | ||
| C. | C的起始浓度越大,K值越大 | D. | K越大,反应进行的程度越大 |
分析 K为生成物浓度幂之积与反应物浓度幂之积的比,K越大,正向进行的趋势越大,K只与温度有关,以此来解答.
解答 解:A.K只与温度有关,与压强无关,压强改变时K不变,故A错误;
B.K越大,正向进行的趋势越大,C的平衡浓度越大,故B错误;
C.K只与温度有关,与C的起始浓度无关,故C错误;
D.K可衡量反应正向进行的趋势,则K越大,反应进行的程度越大,故D正确;
故选D.
点评 本题考查化学平衡常数的含义,为高频考点,把握K的意义及K的影响因素为解答的关键,侧重分析与应用能力的考查,注意K只与温度有关,题目难度不大.

练习册系列答案
相关题目
10.硫酸亚铁易被氧化而变质.为检验某补血剂中硫酸亚铁是否变质,可向该补血剂配成的溶液中加入( )
| A. | AgNO3溶液 | B. | 盐酸酸化的BaCl2溶液 | ||
| C. | KSCN溶液 | D. | HNO3酸化的Ba(NO3)2溶液 |
17.以下对影响反应方向的因素的判断错误的是( )
| A. | 有时焓变起决定性作用 | |
| B. | 有时熵变起决定性作用 | |
| C. | 焓变和熵变是两个主要因素 | |
| D. | 温度不可能对反应方向起决定性作用 |
7.“84”消毒液和漂白粉都是氯气与碱反应在生活中的实际应用,下面说法错误的是( )
| A. | “84”消毒液有漂白和消毒作用 | |
| B. | 工业中将氯气通入石灰乳中制取漂白粉 | |
| C. | 漂白粉的有效成分是CaCl2和Ca(ClO)2 | |
| D. | 漂白粉在空气中久置失效 |
14.用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的是( )
| A. | 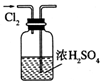 干燥C12 | B. | 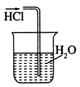 吸收HCl | ||
| C. | 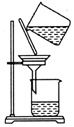 除去粗盐中的不溶物 | D. | 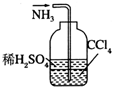 吸收NH3 |
11.下列与有机物相关的说法正确的是( )
| A. | 乙烯能使溴水、酸性高锰酸钾溶液褪色,褪色的本质相同 | |
| B. | 乙烷和乙烯分别与C12反应均有1.2二氯乙烷生成,且反应类型不同 | |
| C. | 油脂、葡萄糖、蛋白质都是人体重要的营养物质,它们都能水解 | |
| D. | 制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
17.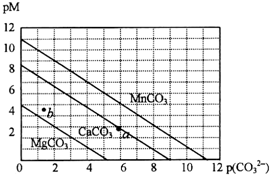 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示.已知:pM=-lg c(M),p(CO32-)=-lg c(CO32-).下列说法正确的是( )
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示.已知:pM=-lg c(M),p(CO32-)=-lg c(CO32-).下列说法正确的是( )
 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示.已知:pM=-lg c(M),p(CO32-)=-lg c(CO32-).下列说法正确的是( )
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示.已知:pM=-lg c(M),p(CO32-)=-lg c(CO32-).下列说法正确的是( )| A. | M离子浓度越大,pM值越大 | |
| B. | MgCO3、CaCO3、MnCO3的Ksp依次增大 | |
| C. | b点表示MgCO3为不饱和溶液,若表示CaCO3则有沉淀析出 | |
| D. | a点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |