题目内容
用下列装置不能达到有关实验目的是( )
A、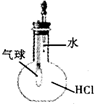 验证HCl的溶解性 |
B、 制备Fe(OH)2 |
C、 干燥并收集NH3 |
D、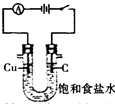 利用电解法制H2和Cl2 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.氯化氢极易溶于水;
B.CCl4的密度比水大;
C.NH3是碱性气体,用碱石灰干燥;
D.电解饱和食盐水时石墨做阳极.
B.CCl4的密度比水大;
C.NH3是碱性气体,用碱石灰干燥;
D.电解饱和食盐水时石墨做阳极.
解答:
解:A.氯化氢极易溶于水,溶于水后,压强减小使气球变大,故A正确;
B.CCl4的密度比水大,不能防止O2将Fe(OH)2氧化,故B错误;
C.NH3是碱性气体,用碱石灰干燥,这样收集气体集气瓶中排除的是空气,并可用倒扣的漏斗吸收尾气,能防止倒吸,故C正确;
D.电解饱和食盐水时石墨做阳极,阳极反应为2Cl--2e-=Cl2↑,阴极反应为2H++2e-=H2↑,故D正确.
故选B.
B.CCl4的密度比水大,不能防止O2将Fe(OH)2氧化,故B错误;
C.NH3是碱性气体,用碱石灰干燥,这样收集气体集气瓶中排除的是空气,并可用倒扣的漏斗吸收尾气,能防止倒吸,故C正确;
D.电解饱和食盐水时石墨做阳极,阳极反应为2Cl--2e-=Cl2↑,阴极反应为2H++2e-=H2↑,故D正确.
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及物质制备、气体的收集和性质实验等,把握实验操作的规范性、实验细节和实验原理为解答的关键,注意方案的合理性、评价性、操作性分析,题目难度不大.

练习册系列答案
相关题目
将99mL 0.5mol?L-1H2SO4溶液与101mL 1mol?L-1NaOH溶液充分混合,混合后溶液的pH约为( )
| A、0.4 | B、2 |
| C、12 | D、13.6 |
关于反应2NaBr+Cl2═2NaCl+Br2,下列说法不正确的是( )
| A、Cl2是氧化剂,反应中Cl原子得到电子 |
| B、当1molCl2完全反应时,有2mol电子发生转移 |
| C、NaBr是还原剂,反应中溴离子得到电子 |
| D、当1molNaBr完全反应时,有1mol电子发生转移 |
下列说法中错误的是( )
| A、NaHCO3溶液中碳元素主要以HCO3-存在 |
| B、Na2CO3溶液中滴加酚酞呈红色,加热红色变深 |
| C、NH4Cl溶液呈酸性这一事实能说明一水合氨为弱碱 |
| D、在稀醋酸中加醋酸钠固体能促进醋酸的电离 |