题目内容
下列离子方程式书写不正确的是( )
| A、Cl2通入烧碱溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
| B、Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-═2AlO2-+H2O |
| C、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| D、FeCl2溶液中通入足量的Cl2:2Fe2++Cl2═2Fe3++2Cl- |
考点:离子方程式的书写
专题:
分析:A.二者反应生成NaCl、NaClO和水;
B.二者反应生成偏铝酸钠和水;
C.Al(OH)3不溶于弱碱溶液且弱电解质写化学式;
D.二者反应生成氯化铁.
B.二者反应生成偏铝酸钠和水;
C.Al(OH)3不溶于弱碱溶液且弱电解质写化学式;
D.二者反应生成氯化铁.
解答:
解:A.二者反应生成NaCl、NaClO和水,离子方程式为Cl2+2OH-═Cl-+ClO-+H2O,故A正确;
B.二者反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-═2AlO2-+H2O,故B正确;
C.Al(OH)3不溶于弱碱溶液且弱电解质写化学式,离子方程式为Al3++3NH3.H2O=Al(OH)3↓+3NH4+,故C错误;
D.二者反应生成氯化铁,离子方程式为2Fe2++Cl2═2Fe3++2Cl-,故D正确;
故选C.
B.二者反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-═2AlO2-+H2O,故B正确;
C.Al(OH)3不溶于弱碱溶液且弱电解质写化学式,离子方程式为Al3++3NH3.H2O=Al(OH)3↓+3NH4+,故C错误;
D.二者反应生成氯化铁,离子方程式为2Fe2++Cl2═2Fe3++2Cl-,故D正确;
故选C.
点评:本题考查离子方程式正误判断,为高考高频点,明确离子性质及离子方程式书写规则即可解答,单质、气体、沉淀、弱电解质、络合物等都写化学式,要注意遵循原子守恒、电荷守恒及转移电子守恒.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂又不是还原剂.下列反应与Cl2+SO2+2H2O=H2SO4+2HCl相比较,水的作用完全相同的是( )
A、2H2O
| ||||
| B、4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||||
| C、2Na+2H2O=2NaOH+H2↑ | ||||
| D、2Na2O2+2H2O=4NaOH+O2↑ |
物质的量相同的甲烷和氨气,一定相等的是( )
| A、体积 | B、质量 |
| C、质子数 | D、原子数 |
若 pH=3 的酸溶液和 pH=11 的碱溶液等体积混合后溶液呈酸性,其原因可能是( )
| A、生成了一种强酸弱碱盐 |
| B、弱酸溶液与强碱溶液反应 |
| C、强酸溶液与强碱溶液反应 |
| D、一元强酸溶液和一元强碱溶液反应 |
下列有关化学用语表示正确的是( )
A、离子结构示意图 只能表示 只能表示
| ||
B、水的球棍模型: | ||
| C、碳酸氢钠在水溶液中的电离方程式:NaHCO3=Na++HCO3- | ||
D、作为相对原子质量标准的碳原子:
|
把Ca(OH)2放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s)?Ca2+(aq)+2OH-(aq).当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是( )
| A、溶液中Ca2+的浓度增大 |
| B、溶液中Ca2+的浓度减小 |
| C、溶液中pH不变 |
| D、溶液中pH增大 |
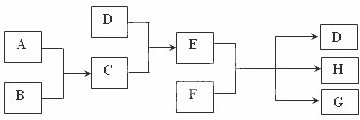
 有一无色溶液,可能含有Fe3+,Al3+,Mg2+,Cu2+,NH4+,K+,CO32-,SO42-,NO3-等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图所示:
有一无色溶液,可能含有Fe3+,Al3+,Mg2+,Cu2+,NH4+,K+,CO32-,SO42-,NO3-等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图所示: