题目内容
| |||||||||||||||||||||||||||||||||
答案:3.C;
解析:
解析:
(1) |
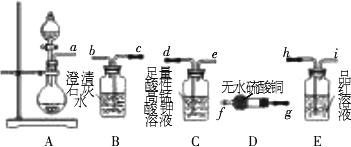
答案: g-f-h-i-d-e-c讲析:水用无水硫酸铜检验,二氧化硫用品红溶液检验,二氧化碳用澄清石灰水检验.由于 Ca(OH)2+SO2 |
(2) |
答案:浓硫酸 白色固体先变为黄褐色,后变为黑色,并膨胀,产生大量气泡 白色粉末变蓝色 讲析:浓硫酸装入分液漏斗,蔗糖装入烧瓶;烧瓶里的现象是:白色蔗糖变成黑色膨胀状固体,同时产生气泡.因为会产生水蒸气,白色无水硫酸铜会变成蓝色. |
(3) |
酸性高锰酸钾溶液吸收二氧化硫,发生氧化还原反应.浓硫酸不能吸收二氧化硫,二氧化硫和二氧化碳都能被氢氧化钠溶液吸收,饱和碳酸氢钠溶液与二氧化硫反应产生二氧化碳,对检验二氧化碳有干扰: NaHCO3+SO2 |
(4) |
答案: E中品红溶液褪色 B中澄清石灰水变浑浊讲析:装置 E中品红溶液褪色,说明反应产物中有二氧化硫;确定二氧化硫除净,B中澄清石灰水变浑浊,能证明产物中有二氧化碳. |
(5) |
答案:浓硫酸溶于水放出大量热量,使混合物温度升高 H2O讲析:浓硫酸遇水放出大量热量,使混合物温度升高,加快反应. 蔗糖遇浓硫酸时发生的化学反应有: C12H22O11(蔗糖)点评:根据实验目的将仪器排序:①制备实验:一般顺序为气体发生装置→气体净化装置→气体干燥装置→主体反应装置→产品收集装置→尾气处理装置;②检验气体产物的仪器顺序:气体发生装置→检验水装置→检验气体 (Ⅰ)→除去气体(Ⅰ)→确认气体(Ⅰ)除净→检验气体(Ⅱ)→尾气处理装置.在连接接口时,洗气瓶应长导管进气,短导管出气;排水集气瓶,应短导管进气,长导管出水;干燥管,应大口进气,小口出气.明白这些常识后,即可根据实验现象判断物质的性质. |

练习册系列答案
相关题目