题目内容
下列实验现象描述正确的是( )
| A、氯化氢与氨气相遇,有大量的白雾生成 |
| B、SO2通入品红溶液,红色褪去,再加热,红色不再出现 |
| C、SO2具有氧化性,可用于漂白纸浆 |
| D、用铂丝蘸取硫酸钠溶液灼烧,火焰呈黄色 |
考点:氯、溴、碘及其化合物的综合应用,二氧化硫的化学性质,焰色反应
专题:元素及其化合物
分析:A、小液滴为雾,固体小颗粒为烟;
B、二氧化硫的漂白原理是和有色物质化合生成无色物质,加热分解后恢复原来颜色;
C、二氧化硫的漂白原理是和有色物质化合生成无色物质,不是因为氧化性的原因;
D、钠的焰色反应为黄色.
B、二氧化硫的漂白原理是和有色物质化合生成无色物质,加热分解后恢复原来颜色;
C、二氧化硫的漂白原理是和有色物质化合生成无色物质,不是因为氧化性的原因;
D、钠的焰色反应为黄色.
解答:
解:A、小液滴为雾,固体小颗粒为烟,氯化氢与氨气反应生成的氯化铵为固体小颗粒,故A错误;
B、二氧化硫的漂白原理是和有色物质化合生成无色物质,加热分解后恢复原来颜色,故B错误;
C、二氧化硫的漂白原理是和有色物质化合生成无色物质,不是因为氧化性的原因,故C错误;
D、钠的焰色反应为黄色,用铂丝蘸取硫酸钠溶液灼烧,火焰呈黄色,故D正确.
故选:D.
B、二氧化硫的漂白原理是和有色物质化合生成无色物质,加热分解后恢复原来颜色,故B错误;
C、二氧化硫的漂白原理是和有色物质化合生成无色物质,不是因为氧化性的原因,故C错误;
D、钠的焰色反应为黄色,用铂丝蘸取硫酸钠溶液灼烧,火焰呈黄色,故D正确.
故选:D.
点评:本题考查烟雾、二氧化硫性质、焰色反应等知识,侧重于基础知识的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
乳酸( )在一定条件下经聚合生成塑料(
)在一定条件下经聚合生成塑料( ),用这种新型塑料制成的餐具,在乳酸菌的作用下,60天内分解成无害物质,最终不会对环境造成污染.在合成该塑料的聚合反应中生成的另一种产物是( )
),用这种新型塑料制成的餐具,在乳酸菌的作用下,60天内分解成无害物质,最终不会对环境造成污染.在合成该塑料的聚合反应中生成的另一种产物是( )
 )在一定条件下经聚合生成塑料(
)在一定条件下经聚合生成塑料( ),用这种新型塑料制成的餐具,在乳酸菌的作用下,60天内分解成无害物质,最终不会对环境造成污染.在合成该塑料的聚合反应中生成的另一种产物是( )
),用这种新型塑料制成的餐具,在乳酸菌的作用下,60天内分解成无害物质,最终不会对环境造成污染.在合成该塑料的聚合反应中生成的另一种产物是( )| A、H2O |
| B、CO2 |
| C、O2 |
| D、H2 |
用镁铝合金制作的窗框、卷帘门、防护栏等物品轻巧、美观、耐用.与上述这些特点无关的镁铝合金的性质是( )
| A、不易生锈 | B、导电性好 |
| C、密度小 | D、强度高 |
下列离子组能大量共存的是( )
| A、Na+ Al3+ AlO2- Cl- |
| B、Mg2+ Al3+ SO42- NO3- |
| C、Ba2+ K+ SO42- NO3- |
| D、Na+ K+ ClO- S2- |
常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如图所示:下列有关说法正确的是( )
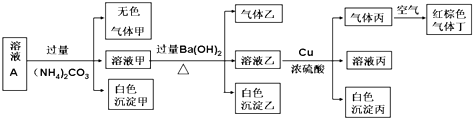

| A、沉淀乙一定有BaCO3,可能有BaSO4 |
| B、实验消耗Cu 14.4g,则生成气体丁的体积为3.36L |
| C、该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子 |
| D、生成的甲、乙、丙气体均为无色的易溶于水气体 |
H2SO3、H2CO3分别属于中强酸和弱酸,H2SO3?H++HSO3-,HSO3-?H++SO32-;H2CO3?H++HCO3-;HCO3-?H++CO32-;电离平衡常数分别为k1、k1′、k2、k2′,已知k1>k1′≈k2>k2′,则溶液中不可以大量共存的离子组合是( )
| A、SO32-、HCO3- |
| B、HSO3-、CO32- |
| C、SO32-、CO32- |
| D、HSO3-、HCO3- |
下列电极反应式正确的是( )
| A、氯碱工业电解饱和食盐水时,阳极电极反应式为 2Cl--2e-=Cl2↑ |
| B、精炼铜时,与电源正极相连的是纯铜,电极反应式为 Cu-2e-=Cu2+ |
| C、氢氧燃料电池的负极反应式 O2+2H2O+4e-=4OH- |
| D、钢铁发生电化腐蚀的正极反应式 Fe-2e-=Fe2+ |