题目内容
碳、硫的含量影响钢铁性能.碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫装置进行测定.
(1)采用图1装置A,在高温下将x克钢样中碳、硫转化为CO2、SO2.
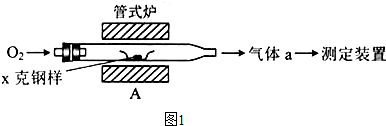
①气体a的成分是 .
②若钢样中碳以FeS形式存在,A中反应:3FeS+5O2
1 +3 .
(2)将气体a通入测硫酸装置中(如图2),采用滴定法测定硫的含量.
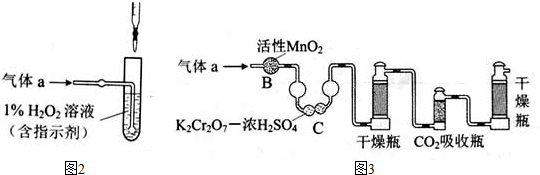
①H2O2氧化SO2的化学方程式:
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液.若消耗1mL NaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数: .
(3)将气体a通入测碳装置中(如图3),采用重量法测定碳的含量.
①气体a通过B和C的目的是
②计算钢样中碳的质量分数,应测量的数据是 .
(1)采用图1装置A,在高温下将x克钢样中碳、硫转化为CO2、SO2.

①气体a的成分是
②若钢样中碳以FeS形式存在,A中反应:3FeS+5O2
| ||
(2)将气体a通入测硫酸装置中(如图2),采用滴定法测定硫的含量.

①H2O2氧化SO2的化学方程式:
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液.若消耗1mL NaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:
(3)将气体a通入测碳装置中(如图3),采用重量法测定碳的含量.
①气体a通过B和C的目的是
②计算钢样中碳的质量分数,应测量的数据是
考点:真题集萃,含硫物质的性质及综合应用,探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)①该装置中C、S和氧气反应生成二氧化碳、二氧化硫,还有部分氧气剩余;
②若钢样中S以FeS形式存在,FeS被氧气氧化,Fe元素化合价由+2价变为+3价,-2价的S被氧化为+4价,结合化学计量数知,生成物是二氧化硫和四氧化三铁;
(2)①双氧水具有强氧化性,二氧化硫具有还原性,二者发生氧化还原反应生成硫酸和水;
②若消耗1mL NaOH溶液相当于硫的质量为y克,z mL NaOH溶液相当于硫的质量为yzg,再根据质量分数公式计算硫的质量分数;
(3)①测定二氧化碳的含量,需要将二氧化硫除去防止造成干扰;
②计算钢样中碳的质量分数,需要测定吸收二氧化碳的质量.
②若钢样中S以FeS形式存在,FeS被氧气氧化,Fe元素化合价由+2价变为+3价,-2价的S被氧化为+4价,结合化学计量数知,生成物是二氧化硫和四氧化三铁;
(2)①双氧水具有强氧化性,二氧化硫具有还原性,二者发生氧化还原反应生成硫酸和水;
②若消耗1mL NaOH溶液相当于硫的质量为y克,z mL NaOH溶液相当于硫的质量为yzg,再根据质量分数公式计算硫的质量分数;
(3)①测定二氧化碳的含量,需要将二氧化硫除去防止造成干扰;
②计算钢样中碳的质量分数,需要测定吸收二氧化碳的质量.
解答:
解:(1)①该装置中C、S在A装置中被氧气反应生成二氧化碳、二氧化硫,还有部分氧气剩余,所以气体a的成分是SO2、CO2、O2,故答案为:SO2、CO2、O2;
②若钢样中S以FeS形式存在,FeS被氧气氧化,Fe元素化合价由+2价变为+3价,-2价的S被氧化为+4价,结合化学计量数知,生成物是二氧化硫和四氧化三铁,所以反应方程式为3FeS+5O2
Fe3O4+3SO2,
故答案为:Fe3O4;SO2;
(2)①双氧水具有强氧化性,二氧化硫具有还原性,二者发生氧化还原反应生成硫酸和水,反应方程式为 H2O2+SO2=H2SO4,故答案为:H2O2+SO2=H2SO4;
②若消耗1mL NaOH溶液相当于硫的质量为y克,z mL NaOH溶液相当于硫的质量为yzg,硫的质量分数为
×100%=
,故答案为:
;
(3)①测定二氧化碳的含量,需要将二氧化硫除去防止造成干扰,B装置可吸收二氧化硫,C装置可以验证二氧化硫是否除尽,所以装置B和C的作用是除去二氧化硫,故答案为:排除二氧化硫对二氧化碳测定的干扰;
②计算钢样中碳的质量分数,需要测定吸收二氧化碳的质量,所以需要测定吸收二氧化碳前后吸收瓶的质量,故答案为:二氧化碳前后吸收瓶的质量.
②若钢样中S以FeS形式存在,FeS被氧气氧化,Fe元素化合价由+2价变为+3价,-2价的S被氧化为+4价,结合化学计量数知,生成物是二氧化硫和四氧化三铁,所以反应方程式为3FeS+5O2
| ||
故答案为:Fe3O4;SO2;
(2)①双氧水具有强氧化性,二氧化硫具有还原性,二者发生氧化还原反应生成硫酸和水,反应方程式为 H2O2+SO2=H2SO4,故答案为:H2O2+SO2=H2SO4;
②若消耗1mL NaOH溶液相当于硫的质量为y克,z mL NaOH溶液相当于硫的质量为yzg,硫的质量分数为
| yzg |
| xg |
| yz |
| x |
| yz |
| x |
(3)①测定二氧化碳的含量,需要将二氧化硫除去防止造成干扰,B装置可吸收二氧化硫,C装置可以验证二氧化硫是否除尽,所以装置B和C的作用是除去二氧化硫,故答案为:排除二氧化硫对二氧化碳测定的干扰;
②计算钢样中碳的质量分数,需要测定吸收二氧化碳的质量,所以需要测定吸收二氧化碳前后吸收瓶的质量,故答案为:二氧化碳前后吸收瓶的质量.
点评:本题考查了C、S含量的测定,涉及氧化还原反应、方程式的配平等知识点,明确实验原理是解本题关键,结合物质的性质来分析解答,题目难度中等.

练习册系列答案
相关题目
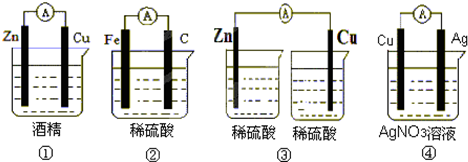
如图所示,关于该装置的下列叙述中,不正确的是( )
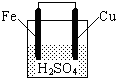

| A、铁棒是负极,发生氧化反应 |
| B、铜棒上有气体放出 |
| C、稀硫酸的pH值不断减小 |
| D、电池总反应方程式可表示为:Fe+2H+=Fe2++H2↑ |
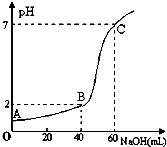 常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示.下列叙述正确的是( )
常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示.下列叙述正确的是( )| A、所用HCl的浓度是0.09mol?L-1,NaOH溶液浓度为0.03mol?L-1 |
| B、在B点,溶液中离子浓度关系为:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C、A、B、C三点水的电离程度大小依次为:A>B>C |
| D、滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低 |
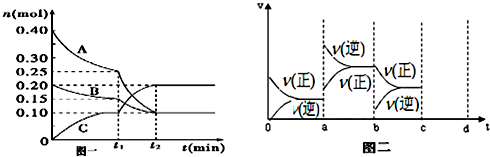
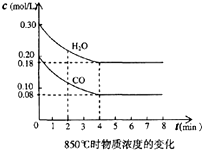 在体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
在体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应: