题目内容
10.将等物质的量的X和Y混合气体,通入密闭容器中发生如下反应:X(g)+2Y(g)?2Z(g),平衡时混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于( )| A. | 33% | B. | 40% | C. | 50% | D. | 67% |
分析 假设X和Y起始物质的量均为1mol,达平衡时消耗Y物质的量为nmol,利用三段式用m表示出平衡时各各组分的物质的量,根据到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2列方程计算n的值,再根据转化率定义计算.
解答 解:假设X和Y物质的量为1mol,达平衡时消耗Y物质的量为nmol,则:
X(g)+2Y(g)?2Z(g)
起始量(mol):1 1 0
变化量(mol):0.5n n n
平衡量(mol):1-0.5n 1-n n
平衡后测得混合气体中反应物的总物质的量与成物的总物质的量之比为3:2,则:(1-0.5n+1-n):n=3:2,
解得:n=$\frac{2}{3}$,
Y的转化率为:$\frac{\frac{2}{3}mol}{1mol}$×100%≈67%,
故选D.
点评 本题化学平衡的有关计算,题目难度中等,明确三段式在化学平衡的计算方法为解答关键,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
20.下列说法中正确的是( )
| A. | 分子通式为CnH2n+2的两烷烃一定互为同系物 | |
| B. | 卤代烃发生水解反应一定生成醇 | |
| C. | 苯和甲苯都能被酸性KMnO4溶液氧化 | |
| D. | 烃类都能燃烧生成CO2和水 |
1.有机化学中取代反应范畴很广,下列4个反应中,属于取代反应范畴的是( )
| A. | 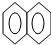 +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$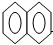 -NO2+H2O -NO2+H2O | |
| B. | CH3CH2CH2CH(OH)CH3$→_{△}^{浓硫酸}$CH3CH2CH=CHCH3+H2O | |
| C. | CH3CHO+H2$→_{催化剂}^{高温高压}$CH3CH2OH | |
| D. | (CH3)2CHCH=CH2+HI→(CH3)2CHCHICH3 |
5.下列中和反应中放出热量最多的是( )
| A. | 100 mL 0.3 mol/L 的HCl 和50 mL 0.3 mol/L 的NaOH相混合 | |
| B. | 80mL 0.3 mol/L 的HCl 和80 mL 0.3 mol/L 的NaOH溶液相混合 | |
| C. | 80mL 0.3 mol/L 的H2SO4 和80 mL 0.3 mol/L 的NaOH溶液相混合 | |
| D. | 50mL 0.3 mol/L 的H2SO4 和50 mL 0.6 mol/L 的NaOH溶液相混合 |
15.少量铁粉与100mL 0.01mol•L-1的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法的( )
①加H2O
②滴入几滴CuSO4
③滴入几滴浓盐酸
④加CH3COONa固体
⑤加NaCl固体
⑥升高温度(不考虑盐酸挥发)
⑦改用10mL 0.1mol•L-1盐酸.
①加H2O
②滴入几滴CuSO4
③滴入几滴浓盐酸
④加CH3COONa固体
⑤加NaCl固体
⑥升高温度(不考虑盐酸挥发)
⑦改用10mL 0.1mol•L-1盐酸.
| A. | ①⑥⑦ | B. | ③⑤⑦ | C. | ③⑥⑦ | D. | ⑤⑥⑦ |
2.珍爱生命,远离毒品.以下是四种毒品的结构简式,下列有关说法正确的是( )
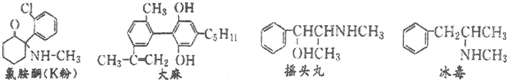

| A. | 四种毒品中都含有苯环,都属于芳香烃 | |
| B. | K粉的化学式为C13H15ONCl | |
| C. | 摇头丸经过消去反应、加成反应可制取冰毒 | |
| D. | 1mol大麻与溴水反应最多消耗4molBr2 |
19.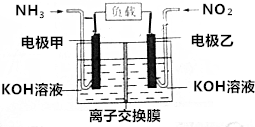 人民网北京2015年12月1日电,为了应对持续的雾霾天气,京津冀区域多个城市迅速启动应急响应,落实应对措施.雾霾成分中含有氮的氧化物,利用反应NO2+NH3→N2+H2O制作如图所示的电池,用以消除氮氧化物的污染.下列有关该电池的说法一定正确的是( )
人民网北京2015年12月1日电,为了应对持续的雾霾天气,京津冀区域多个城市迅速启动应急响应,落实应对措施.雾霾成分中含有氮的氧化物,利用反应NO2+NH3→N2+H2O制作如图所示的电池,用以消除氮氧化物的污染.下列有关该电池的说法一定正确的是( )
 人民网北京2015年12月1日电,为了应对持续的雾霾天气,京津冀区域多个城市迅速启动应急响应,落实应对措施.雾霾成分中含有氮的氧化物,利用反应NO2+NH3→N2+H2O制作如图所示的电池,用以消除氮氧化物的污染.下列有关该电池的说法一定正确的是( )
人民网北京2015年12月1日电,为了应对持续的雾霾天气,京津冀区域多个城市迅速启动应急响应,落实应对措施.雾霾成分中含有氮的氧化物,利用反应NO2+NH3→N2+H2O制作如图所示的电池,用以消除氮氧化物的污染.下列有关该电池的说法一定正确的是( )| A. | 电极乙为电池负极 | |
| B. | 离子交换膜为质子交换膜 | |
| C. | 负极反应式为2NH3-6e-+6OH-═N2+6H2O | |
| D. | 28.0L(标准状况)NO2完全处理,转移5mol电子 |
4.1932年美国化学家鲍林首先提出了电负性的概念.电负性(用X表示也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
①预测元素周期表中,X值最小的元素位置和名称:第六周期第IA族,铯(放射性元素除外).
②根据表中的所给数据分析,同周期内的不同元素X的值变化的规律是随着原子序数的增大而增大
通过分析X值变化规律,确定P、Mg 的X值范围:1.7<X(P)<2.3,1.5<X(Mg)<0.9.
③经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlCl3、Al2O3中形成的化学键的类型分别为共价键、离子键(填离子键或共价键)
④根据所学分子的立体构型和杂化方式来填写下列表格
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.5 | 1.7 | 2.3 | 3.0 | 0.8 |
①预测元素周期表中,X值最小的元素位置和名称:第六周期第IA族,铯(放射性元素除外).
②根据表中的所给数据分析,同周期内的不同元素X的值变化的规律是随着原子序数的增大而增大
通过分析X值变化规律,确定P、Mg 的X值范围:1.7<X(P)<2.3,1.5<X(Mg)<0.9.
③经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlCl3、Al2O3中形成的化学键的类型分别为共价键、离子键(填离子键或共价键)
④根据所学分子的立体构型和杂化方式来填写下列表格
| 微粒 | BeCl2 | H2S | NH3 | CO32- | BF3 |
| 中心原子杂化方式 | |||||
| 微粒的空间构型 |