题目内容
下列化合物①HCl②NaOH③CH2COOH④NH2.H2O⑤CH3COONa⑥NH4Cl⑦C2H4OH⑧SO2
(1)属于非电解质的是 ,溶液呈酸性的有 (填序号)
(2)常温下0.1mol.L-1NaOH溶液的pH= ,pH=2的NH4Cl溶液中由水电离产生的c(H+)=
(3)用离子方程式表示CH2COONa溶液呈碱性的原因 含等物质的量的③和⑤的混合溶液中离子浓度按由大小的顺序为
(4)常温下,向100mI,0.01mol.L-1HA溶液滴加入0.02mol.L-1MOH溶液.图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计),回答下列问题:

①由图中信息可知HA为 酸(填“强”或“弱”)
②在滴加过程中,水的电离程度的变化是先 后 (填“增大”“减小”或“不变”)
③K点对应的溶液中c(M+)+c(MOH)= mol.L-1
(5)在25℃下,向浓度均为0.01mol.L-1
的FeCl2和CuCl2混合溶液中逐滴加氨水先生成 沉淀(填化学式),当测得溶液pH=11时,则此温度下残留在溶液中的c(Cu2+).c(Fe3+)= 已知(25℃时Ksp[Fe(OH2)=4.0×1028,Ksp[Cu(OH)2]=2.2×10-29)
(6)25℃时,将bmolNH4NO3溶于水,向该溶液滴加aL氨水后溶液呈中性,则所滴加氨水的浓度为 mol.L-1(已知Kb(NH2.H2O)=2×10-2mol.L-1)
(1)属于非电解质的是
(2)常温下0.1mol.L-1NaOH溶液的pH=
(3)用离子方程式表示CH2COONa溶液呈碱性的原因
(4)常温下,向100mI,0.01mol.L-1HA溶液滴加入0.02mol.L-1MOH溶液.图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计),回答下列问题:

①由图中信息可知HA为
②在滴加过程中,水的电离程度的变化是先
③K点对应的溶液中c(M+)+c(MOH)=
(5)在25℃下,向浓度均为0.01mol.L-1
的FeCl2和CuCl2混合溶液中逐滴加氨水先生成
(6)25℃时,将bmolNH4NO3溶于水,向该溶液滴加aL氨水后溶液呈中性,则所滴加氨水的浓度为
考点:酸碱混合时的定性判断及有关ph的计算,弱电解质在水溶液中的电离平衡,难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)在水溶液和熔融状态下都不导电的化合物为非电解质;酸或酸式盐或强酸弱碱盐的溶液显示酸性;
(2)根据pH=-lgc(H+)计算出0.1mol/L的氢氧化钠溶液的pH;氯化铵溶液中的氢离子来自水的电离;
(3)醋酸钠是强碱弱酸盐,醋酸根离子水解而使其溶液呈碱性,根据电荷守恒确定离子浓度大小;
(4)①根据酸的浓度和溶液的PH判断酸的强弱;
②根据酸、碱溶液抑制了水的电离,氢离子或氢氧根离子浓度越大,抑制程度越大分析;
③根据物料守恒计算;
(5)溶度积常数小的物质先沉淀,根据溶度积常数结合溶液中氢氧根离子浓度计算c(Cu2+):c(Fe3+);
(6)依据一水合氨的电离平衡常数计算得到氨水浓度.
(2)根据pH=-lgc(H+)计算出0.1mol/L的氢氧化钠溶液的pH;氯化铵溶液中的氢离子来自水的电离;
(3)醋酸钠是强碱弱酸盐,醋酸根离子水解而使其溶液呈碱性,根据电荷守恒确定离子浓度大小;
(4)①根据酸的浓度和溶液的PH判断酸的强弱;
②根据酸、碱溶液抑制了水的电离,氢离子或氢氧根离子浓度越大,抑制程度越大分析;
③根据物料守恒计算;
(5)溶度积常数小的物质先沉淀,根据溶度积常数结合溶液中氢氧根离子浓度计算c(Cu2+):c(Fe3+);
(6)依据一水合氨的电离平衡常数计算得到氨水浓度.
解答:
解:(1)①HCl②NaOH③CH2COOH④NH2?H2O⑤CH3COONa⑥NH4Cl⑦C2H4OH⑧SO2,以上各物质中,在水溶液和熔融状态下都不导电的化合物有:⑦⑧;溶液显示酸性的有:①③⑥⑧,
故答案为:⑦⑧;①③⑥⑧;
(2)常温下0.1mol/LNaOH溶液中氢离子浓度为:10-13mol/L,该溶液的pH=13;pH=2的NH4Cl溶液中氢离子浓度为0.01mol/L,该溶液中铵根离子水解促进了水的电离,则由水电离产生的c(H+)=0.01mol/L,
故答案为:13;0.01mol/L;
(3)醋酸钠是强碱弱酸盐,醋酸根离子水解生成醋酸,导致溶液中氢氧根离子浓度大于氢离子浓度而使其溶液呈碱性,水解离子方程式为:CH3COO?+H2O?CH3COOH+OH?,溶液呈碱性,所以c(OH-)>c(H+),溶液中存在电荷守恒,c(Na+)+c(H+)=c(CH3COO?)+c(OH-),则c(Na+)>c(CH3COO?),所以离子浓度大小顺序是c(Na+)>c(CH3COO?)>c(OH-)>c(H+),
故答案为:CH3COO?+H2O?CH3COOH+OH?;c(Na+)>c(CH3COO?)>c(OH-)>c(H+);
(4)根据图象知,0.01mol?L-1HA溶液中PH=2,氢离子浓度等于酸浓度,所以该酸是强酸,
故答案为:强;
②酸溶液中氢离子抑制了水的电离,随着碱溶液的加入,溶液中氢离子浓度逐渐减小,水的电离程度逐渐增大,当恰好反应后,再滴加碱溶液,碱溶液中氢氧根离子抑制了水的电离,且碱的浓度越大,抑制程度越大,所以水的电离程度变化为:先增大后减小,
故答案为:增大;减小;
③K点时,加入的MOH的物质的量=0.02mol?L-1×0.1L=0.002mol,混合溶液的体积是0.2L,根据物料守恒知,c(M+)+c(MOH)=
=0.01mol/L,
故答案为:0.01.
(5)溶度积常数越小的越先沉淀,根据溶度积常数知,先生成沉淀的是Fe(OH)3,当溶液的pH=11时,c(OH-)=1×10-3mol/L,c(Cu2+):c(Fe3+)=
:
=5.5×1014,
故答案为:Fe(OH)3;5.5×1014;
(6)在该溶液中,存在电荷守恒:c(NH4+)+(H+)=c(NO3-)+c(OH-),由于溶液为中性,则(H+)=c(OH-),所以c(NH4+)=c(NO3-),由于Kb(NH3?H2O)=2.0×10-5mol/L,即:Kb=
=2.0×10-5mol/L,
设加入的氨水物质的量为n,混合液体积为V,由于c(NH4+)=c(NO3-),相当于溶液中的一水合氨完全来自滴加的氨水,
则c(NH3?H2O)=
=
=
,
解得:n(NH3?H2O)=
mol,
所以滴加的氨水的浓度为:c(NH3?H2O)=
mol/L=
mol/L,
故答案为:
mol/L.
故答案为:⑦⑧;①③⑥⑧;
(2)常温下0.1mol/LNaOH溶液中氢离子浓度为:10-13mol/L,该溶液的pH=13;pH=2的NH4Cl溶液中氢离子浓度为0.01mol/L,该溶液中铵根离子水解促进了水的电离,则由水电离产生的c(H+)=0.01mol/L,
故答案为:13;0.01mol/L;
(3)醋酸钠是强碱弱酸盐,醋酸根离子水解生成醋酸,导致溶液中氢氧根离子浓度大于氢离子浓度而使其溶液呈碱性,水解离子方程式为:CH3COO?+H2O?CH3COOH+OH?,溶液呈碱性,所以c(OH-)>c(H+),溶液中存在电荷守恒,c(Na+)+c(H+)=c(CH3COO?)+c(OH-),则c(Na+)>c(CH3COO?),所以离子浓度大小顺序是c(Na+)>c(CH3COO?)>c(OH-)>c(H+),
故答案为:CH3COO?+H2O?CH3COOH+OH?;c(Na+)>c(CH3COO?)>c(OH-)>c(H+);
(4)根据图象知,0.01mol?L-1HA溶液中PH=2,氢离子浓度等于酸浓度,所以该酸是强酸,
故答案为:强;
②酸溶液中氢离子抑制了水的电离,随着碱溶液的加入,溶液中氢离子浓度逐渐减小,水的电离程度逐渐增大,当恰好反应后,再滴加碱溶液,碱溶液中氢氧根离子抑制了水的电离,且碱的浓度越大,抑制程度越大,所以水的电离程度变化为:先增大后减小,
故答案为:增大;减小;
③K点时,加入的MOH的物质的量=0.02mol?L-1×0.1L=0.002mol,混合溶液的体积是0.2L,根据物料守恒知,c(M+)+c(MOH)=
| 0.002mol |
| 0.2L |
故答案为:0.01.
(5)溶度积常数越小的越先沉淀,根据溶度积常数知,先生成沉淀的是Fe(OH)3,当溶液的pH=11时,c(OH-)=1×10-3mol/L,c(Cu2+):c(Fe3+)=
| 2.2×10-20 |
| (10-3)2 |
| 4.0×10-38 |
| (10-3)3 |
故答案为:Fe(OH)3;5.5×1014;
(6)在该溶液中,存在电荷守恒:c(NH4+)+(H+)=c(NO3-)+c(OH-),由于溶液为中性,则(H+)=c(OH-),所以c(NH4+)=c(NO3-),由于Kb(NH3?H2O)=2.0×10-5mol/L,即:Kb=
| c(NH+4)?c(OH-) |
| c(NH3?H2O) |
设加入的氨水物质的量为n,混合液体积为V,由于c(NH4+)=c(NO3-),相当于溶液中的一水合氨完全来自滴加的氨水,
则c(NH3?H2O)=
| n |
| V |
| c(NH4+)?c(OH-) |
| Kb |
| ||
| 2.5×10-5 |
解得:n(NH3?H2O)=
| b |
| 200 |
所以滴加的氨水的浓度为:c(NH3?H2O)=
| ||
| a |
| b |
| 200a |
故答案为:
| b |
| 200a |
点评:本题考查较综合,涉及酸碱混合溶液定性判断、离子浓度大小比较、盐类水解、电解质的判断、溶度积常数的计算等知识点,题目难度中等,根据基本概念结合盐类水解、弱电解质的电离特点来分析解答,难点是(6)题,根据电离平衡常数进行计算即可.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
下列叙述中正确的是( )
| A、氧化还原反应的本质是化合价发生变化 |
| B、有单质产生的分解反应一定是氧化还原反应 |
| C、在同一氧化还原反应中,反应物和生成物中都有氧化剂 |
| D、还原剂在反应中失去电子发生还原反应 |

 ) ②能与FeCl3溶液发生显色反应
) ②能与FeCl3溶液发生显色反应
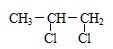 为主要原料(无机试剂任用)制备
为主要原料(无机试剂任用)制备 的合成路线流程图(须注明反应条件)
的合成路线流程图(须注明反应条件)
 有多种同分异构体,写出同分异构体中所有含有1个醛基和2个羟基的芳香族化合物的结构简式
有多种同分异构体,写出同分异构体中所有含有1个醛基和2个羟基的芳香族化合物的结构简式
 (B2H6为乙硼烷)
(B2H6为乙硼烷)

 的合成路线流程图.
的合成路线流程图.