题目内容
16.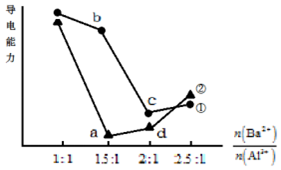 向两份20mL 0.1mol/L Ba(OH)2溶液中各加入一定量的KAl(SO4)2和Al2(SO4)3,溶液的导电性随$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$(混合前)的变化关系如右图所示.下列分析不正确的是( )
向两份20mL 0.1mol/L Ba(OH)2溶液中各加入一定量的KAl(SO4)2和Al2(SO4)3,溶液的导电性随$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$(混合前)的变化关系如右图所示.下列分析不正确的是( )| A. | ①代表加入KAl(SO4)2的变化曲线 | |
| B. | a点溶液的pH值约为7 | |
| C. | b点溶液中大量存在的阳离子有Al3+和Ba2+ | |
| D. | c、d两点溶液中Ba(OH)2均已完全反应 |
分析 A、当$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$=$\frac{3}{2}$时,Ba(OH)2溶液中滴入KAl(SO4)2首先恰好完全反应生成氢氧化铝沉淀和的硫酸钡沉淀,随氢氧化钡的滴加氢氧化铝溶解生成偏铝酸钾,当$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$=$\frac{2}{1}$时恰好完全反应,所以在完全反应前出现两次拐点;
B、a点溶液中$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$=$\frac{3}{2}$,如果 Ba(OH)2为3mol和则Al2(SO4)3为1mol,两者恰好完全反应生成2mol氢氧化铝沉淀和3mol的硫酸钡沉淀;
C、b点$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$=$\frac{3}{2}$时,Ba(OH)2溶液中滴入KAl(SO4)2首先恰好完全反应生成氢氧化铝沉淀和的硫酸钡沉淀,溶液中没有大量存在的阳离子有Al3+和Ba2+;
D、c点Ba(OH)2溶液中滴入KAl(SO4)2恰好完全反应生成偏铝酸钾和硫酸钡,而d点 Ba(OH)2和Al2(SO4)3的物质的量之比为:2:1,硫酸铝过量,氢氧化钡完全反应.
解答 解:A、当$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$=$\frac{3}{2}$时,Ba(OH)2溶液中滴入KAl(SO4)2首先恰好完全反应生成氢氧化铝沉淀和的硫酸钡沉淀,随氢氧化钡的滴加氢氧化铝溶解生成偏铝酸钾,当$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$=$\frac{2}{1}$时恰好完全反应,所以在完全反应前出现两次拐点,所以①代表加入KAl(SO4)2的变化曲线,故A正确;
B、a点溶液中$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$=$\frac{3}{2}$,如果 Ba(OH)2为3mol和则Al2(SO4)3为1mol,两者恰好完全反应生成2mol氢氧化铝沉淀和3mol的硫酸钡沉淀,水溶液呈中性,故B正确;
C、b点$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$=$\frac{3}{2}$时,Ba(OH)2溶液中滴入KAl(SO4)2首先恰好完全反应生成氢氧化铝沉淀和的硫酸钡沉淀,溶液中没有大量存在的阳离子有Al3+和Ba2+,故C错误;
D、c点Ba(OH)2溶液中滴入KAl(SO4)2恰好完全反应生成偏铝酸钾和硫酸钡,而d点 Ba(OH)2和Al2(SO4)3的物质的量之比为:2:1,硫酸铝过量,氢氧化钡完全反应,所以c、d两点溶液中Ba(OH)2均已完全反应,故D正确;
故选C.
点评 本题对于该类图象题应该注意每段图象发生的化学反应,写出化学方程式根据方程式找出量的关系进行计算.

| A. | 常温常压下,1.56g Na2O2含有的阴离子数为0.02NA | |
| B. | 过氧化钠与二氧化碳反应产生氧气0.2mol,则转移0.8NA电子 | |
| C. | 0.1mol铁与高温水蒸汽反应,转移0.3NA电子 | |
| D. | 标准状况下,22.4L CCl4含有的分子数为NA |
| A. | 含有羟基的化合物一定属于醇类 | |
| B. | 苯酚可以使紫色石蕊试液变红 | |
| C. | 分子中含有苯环和羟基的化合物一定是酚 | |
| D. | Na2O2、苯酚久置于空气中,颜色均有变化 |
| A. | P | B. | Mg | C. | Al | D. | Fe |
| A. | 标准状况下,22.4L乙烯中含有的共用电子对数为6NA | |
| B. | 1L pH=13的氢氧化钡溶液中含有的OH-离子数为0.2NA | |
| C. | 46g的无水乙醇与足量乙酸在浓硫酸中加热,可生成88g乙酸乙酯 | |
| D. | 在反应KIO3+6HI═KI+3I2+3H2O中,若有1molH2O生成,则转移电子数为2NA |
| A. | 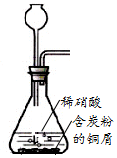 用装置制取NO | |
| B. |  用装置收集NO | |
| C. | 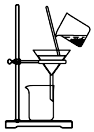 用装置分离炭粉和硝酸铜溶液 | |
| D. | 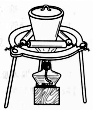 用装置蒸干硝酸铜溶液制Cu(NO3)2•3H2O |
| A. | 水蒸气通过炽热的铁,生成Fe2O3和H2 | |
| B. | 用湿润的淀粉碘化钾试纸检验某气体,试纸变蓝,该气体一定是Cl2 | |
| C. | 除去NO中混有的少量NO2,可将混合气体通过盛有水的洗气瓶,再用排空气法收集NO | |
| D. | 反应MnO2+ZnS+2H2SO4═MnSO4+ZnSO4+S+2H2O中,每析出12.8 g S共转移0.8mol |
| A. | 0.4mol•L-1 | B. | 0.6mol•L-1 | C. | 0.8mol•L-1 | D. | 1.1mol•L-1 |