题目内容
下列说法正确的是( )
| A、一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的△H<0,△S>0 |
| B、在相同条件下,pH=2的强酸和pH=12的强碱发生反应,反应热是定值 |
| C、碳酸氢钠是强电解质,该盐水溶液不存在电离平衡 |
D、在体积一定的绝热容器中发生可逆反应,其正反应速率随时间变化如图所示,则该反应是放热反应 |
考点:焓变和熵变,反应热和焓变,强电解质和弱电解质的概念
专题:基本概念与基本理论
分析:A、Mg与氯气反应放热,其逆反应吸热;
B、反应热的数值与反应物多少有关;
C、碳酸氢钠虽然完全电离,但碳酸氢根不能完全电离,且存在水的电离平衡;
D、反应速率先变大后变小,可知放热导致反应速率增大.
B、反应热的数值与反应物多少有关;
C、碳酸氢钠虽然完全电离,但碳酸氢根不能完全电离,且存在水的电离平衡;
D、反应速率先变大后变小,可知放热导致反应速率增大.
解答:
解:A、Mg与氯气反应放热,其逆反应吸热,△H>0,故A错误;
B、生成1mol水和生成10mol水放热显然是不同的;另外,硫酸与氢氧化钡反应除生成水之外,还有硫酸钡沉淀生成,生成沉淀也要放热,故B错误;
C、碳酸氢钠溶液中存在碳酸氢根的电离平衡和水的电离平衡,故C错误;
D、反应开始,反应速率增大,之后反应速率减小,说明反应刚开始时温度升高对反应速率的影响大于浓度减小对反应速率的影响,说明该反应为放热反应,故D正确.
故选:D.
B、生成1mol水和生成10mol水放热显然是不同的;另外,硫酸与氢氧化钡反应除生成水之外,还有硫酸钡沉淀生成,生成沉淀也要放热,故B错误;
C、碳酸氢钠溶液中存在碳酸氢根的电离平衡和水的电离平衡,故C错误;
D、反应开始,反应速率增大,之后反应速率减小,说明反应刚开始时温度升高对反应速率的影响大于浓度减小对反应速率的影响,说明该反应为放热反应,故D正确.
故选:D.
点评:本题考查反应热与反应物多少的关系、弱电解质的电离平衡、影响化学反应速率的因素,题目跨度大,有一定难度.

练习册系列答案
相关题目
“下列食品添加剂与类别对应正确的是( )
| A、着色剂-苯甲酸钠 |
| B、调味剂-亚硝酸盐 |
| C、营养强化剂-粮食制品加赖氨酸 |
| D、防腐剂--胭脂红 |
下列变化需要加入还原剂才能实现的是( )
| A、Fe3+→Fe2+ |
| B、HCl→Cl2 |
| C、Fe→Fe2+ |
| D、C→CO2 |
下列各组食谱中,营养相对较为平衡的是( )
| A、鸡蛋、牛奶、红烧鱼、豆腐、豆浆、米饭 |
| B、牛肉、猪肝、大豆、羊排、火腿、米饭 |
| C、牛奶、西红柿、米饭、白菜、鸡蛋、青椒炒牛肉、苹果 |
| D、白菜、凉拌黄瓜、西红柿、玉米、米饭、苹果、香蕉 |
下列说法中正确的是( )
| A、由不同种元素组成的物质叫做化合物 |
| B、水溶液中能电离出H+的化合物一定是酸 |
| C、含有氧元素的物质一定就是氧化物 |
| D、酸式盐可以看做是酸分子中的H被金属阳离子或NH4+不完全取代的产物 |
1mol MgCl2中含有( )
| A、3.01×1023个Mg2+ |
| B、6.02×1023个Cl- |
| C、1 mol Mg2+ |
| D、1molCl-离子 |
在一个固定容积的密闭容器中,可发生以下反应:A(g)+B(g)?xC(g)符合图(a)所示的关系(W(C)表示C的体积分数),由此推断关于图(b)的说法正确的是( )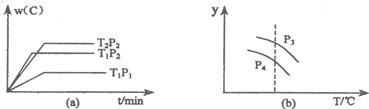

| A、P3>P4,y轴表示A的转化率 |
| B、P3<P4,y轴表示B的体积分数 |
| C、P3>P4,y轴表示混合气体C的体积分数 |
| D、P3<P4,y轴表示混合气体的密度 |
下列物质中存在分子间作用力的是( )
| A、氯化钠 | B、干冰 | C、金刚石 | D、铁 |
下列溶液中微粒的物质的量浓度关系一定正确的是( )
| A、pH=3的NaNO3和盐酸的混合溶液中:c(Na+)=c(Cl-) |
| B、0.1 mol?L-1 NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C、物质的量浓度相等的HCN(弱酸)和NaCN溶液等体积混合后有:c(HCN)+2c(H+)=2c(OH-)+c(CN-) |
| D、0.2mol?L-1 CH3COONa溶液和0.1mol HCl溶液等体积混合后:c(CH3COO-)>c(Na+)>c(Cl-)>c(H+)>c(OH-) |