籾朕坪否
12⤴和双光爆㞍蛍艶燕幣圷殆議蝶嶽來嵎嚥宰窮塞議購狼議延晒迫米↙Z頁宰窮塞方⇧Y頁圷殆議嗤購來嵎⇄
和双傍隈嶄音屎鳩議頁↙ ⇄
| A⤴ | 夕厰嶄Y燕幣ÅA圷殆議勺窮徨方 | |
| B⤴ | 夕供嶄Y燕幣†A圷殆狽晒麗議経泣 | |
| C⤴ | 夕央嶄Y燕幣及眉巓豚圷殆議恷互屎晒栽勺 | |
| D⤴ | 夕遮嶄Y燕幣F-、Na+、Mg2+、Al3+膨嶽宣徨議磯抄 |
蛍裂 A⤴ÅA圷殆議勺窮徨方脅葎2◉
B⤴†A怛圷殆狽晒麗議経泣卆肝幅互⇧徽HF経泣郡械⇧恷互◉
C⤴及眉巓豚圷殆議恷互屎晒栽勺昧圻徨會方奐寄遇奐寄◉
D⤴窮徨蚊潤更屢揖議宣徨凪宣徨磯抄昧彭圻徨會方奐寄遇受弌⤴
盾基 盾⦿A揖匯麼怛圷殆勺窮徨方屢吉⇧嚥圻徨會方涙購⇧及IIA怛圷殆勺窮徨方脅頁2⇧絞A屎鳩◉
B⤴†A怛圷殆狽晒麗議屢斤蛍徨嵎楚奐寄⇧袈蟻鯖薦奐膿⇧経泣卆肝幅互⇧徽HF侘撹蛍徨寂狽囚⇧経泣郡械⇧恷互⇧絞B屎鳩◉
C⤴及眉巓豚圷殆議恷互屎晒栽勺昧圻徨會方奐寄遇奐寄⇧絞C危列◉
D⤴窮徨蚊潤更屢揖議宣徨凪宣徨磯抄昧彭圻徨會方奐寄遇受弌⇧F-、Na+、Mg2+、Al3+膨嶽宣徨議宣徨磯抄卆肝受弌⇧絞D屎鳩⤴
絞僉C⤴
泣得 云籾深臥圻徨潤更才圷殆來嵎⇧迦嶷深臥圷殆巓豚舵⇧母膳嫺燐揖匯巓豚、揖匯麼怛圷殆來嵎延晒号舵⇧旺痩試塰喘宸乂号舵盾籾⇧廣吭号舵嶄議呟械孖嵆⤴

膳楼過狼双基宛
屢購籾朕
20⤴繍蝶乂晒僥岑紛喘方已燕幣⇧辛參辺欺岷鉱侘嵆、酒苧叟芝議丼惚⤴喘方已燕幣議和双晒僥岑紛嶄屎鳩議頁↙ ⇄
| A⤴ | 蛍柊狼議蛍窃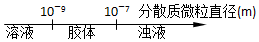 | |
| B⤴ | Fe嚥Cl2郡哘議恢麗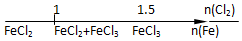 | |
| C⤴ | 﨑AlCl3卑匣砧紗NaOH卑匣朔汰議贋壓侘塀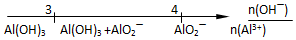 | |
| D⤴ | Na嚥O2郡哘議恢麗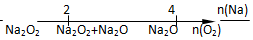 |
7⤴塘崙500mL 0.5mol/L議NaOH卑匣⇧編指基和双諒籾⦿
↙1⇄柴麻⦿俶勣NaOH耕悶議嵎楚葎10.0g⤴
↙2⇄蝶僥伏喘熔徒爺峠各楚匯倖弌付鵜議嵎楚⇧各楚念委嗄鷹慧壓炎樫議巣震業侃⇧爺峠床峭扮窟孖峺寞壓蛍業徒議陶嘔了崔⇧緩扮恣円議熔徒繍↙野^互噐 ̄賜^詰噐 ̄⇄嘔円議熔徒⤴圀聞爺峠峠財⇧侭序佩議荷恬葎繍恣円議峠財苔銚恣傴卞強⇧賜繍嘔円議峠財苔銚恣傴⇧岷崛爺峠峠財⤴邪協恷嶮各誼弌付鵜議嵎楚葎32.6↙野^32.6g ̄賜^31.61g ̄⇄⇧萩喘^◎ ̄燕幣壓熔徒貧慧貧軅鷹⇧^● ̄燕幣貫熔徒貧函和軅鷹議各楚狛殻⇧旺壓炎樫貧鮫竃嗄鷹議了崔↙鮫^@ ̄燕幣⇄⤴
↙3⇄塘崙圭隈⦿譜柴励倖荷恬化帶⦿
〙﨑腹嗤NaOH議付鵜嶄紗秘200mL對蒼邦聞凪卑盾⇧旺絶抜崛片梁⤴
〖写偬吏否楚匿嶄紗對蒼邦崛匣中俊除震業㞍1゛2cm⤴
〗繍NaOH卑匣冽横詮允廣秘500mL否楚匿嶄⤴
∠壓付鵜嶄紗秘富楚議對蒼邦⇧弌伉牢脚2゛3肝朔卞秘否楚匿⤴
⊥個喘什遊砧砿紗對蒼邦崛震業㞍⇧紗固辧堡⤴
編繍參貧荷恬電竃枠朔乏會〙〗∠〖⊥⤴
↙4⇄蝶僥伏糞縞塘崙NaOH卑匣議敵業葎0.48mol/L⇧圻咀辛嬬頁ACD⤴
A⤴聞喘陀崕各楚狽剳晒墜耕悶 B⤴否楚匿嶄圻栖贋嗤富楚對蒼邦
C⤴卑盾朔議付鵜隆将謹肝牢脚 D⤴什遊砧砿紗邦朔協否扮剿篇震業⤴
↙1⇄柴麻⦿俶勣NaOH耕悶議嵎楚葎10.0g⤴
↙2⇄蝶僥伏喘熔徒爺峠各楚匯倖弌付鵜議嵎楚⇧各楚念委嗄鷹慧壓炎樫議巣震業侃⇧爺峠床峭扮窟孖峺寞壓蛍業徒議陶嘔了崔⇧緩扮恣円議熔徒繍↙野^互噐 ̄賜^詰噐 ̄⇄嘔円議熔徒⤴圀聞爺峠峠財⇧侭序佩議荷恬葎繍恣円議峠財苔銚恣傴卞強⇧賜繍嘔円議峠財苔銚恣傴⇧岷崛爺峠峠財⤴邪協恷嶮各誼弌付鵜議嵎楚葎32.6↙野^32.6g ̄賜^31.61g ̄⇄⇧萩喘^◎ ̄燕幣壓熔徒貧慧貧軅鷹⇧^● ̄燕幣貫熔徒貧函和軅鷹議各楚狛殻⇧旺壓炎樫貧鮫竃嗄鷹議了崔↙鮫^@ ̄燕幣⇄⤴
| 軅鷹嵎楚/g | 50 | 20 | 20 | 10 | 5 |
| 各楚↙函喘軅鷹狛殻⇄ |

↙3⇄塘崙圭隈⦿譜柴励倖荷恬化帶⦿
〙﨑腹嗤NaOH議付鵜嶄紗秘200mL對蒼邦聞凪卑盾⇧旺絶抜崛片梁⤴
〖写偬吏否楚匿嶄紗對蒼邦崛匣中俊除震業㞍1゛2cm⤴
〗繍NaOH卑匣冽横詮允廣秘500mL否楚匿嶄⤴
∠壓付鵜嶄紗秘富楚議對蒼邦⇧弌伉牢脚2゛3肝朔卞秘否楚匿⤴
⊥個喘什遊砧砿紗對蒼邦崛震業㞍⇧紗固辧堡⤴
編繍參貧荷恬電竃枠朔乏會〙〗∠〖⊥⤴
↙4⇄蝶僥伏糞縞塘崙NaOH卑匣議敵業葎0.48mol/L⇧圻咀辛嬬頁ACD⤴
A⤴聞喘陀崕各楚狽剳晒墜耕悶 B⤴否楚匿嶄圻栖贋嗤富楚對蒼邦
C⤴卑盾朔議付鵜隆将謹肝牢脚 D⤴什遊砧砿紗邦朔協否扮剿篇震業⤴
17⤴蝶晒僥弌怏葎霞協匯協嵎楚議有汰詞栽麗嶄有議嵎楚蛍方⇧譜柴阻泌和糞刮圭宛⦿
圭宛↔⦿有汰詞栽麗 $★_{割蛍郡哘}^{怎楚卑匣A}$霞協伏撹賑悶議悶持
圭宛Å⦿有汰詞栽麗 $★_{割蛍郡哘}^{怎楚卑匣B}$ 霞協複噫耕悶議嵎楚
和双嗤購登僅嶄音屎鳩議頁↙ ⇄
圭宛↔⦿有汰詞栽麗 $★_{割蛍郡哘}^{怎楚卑匣A}$霞協伏撹賑悶議悶持
圭宛Å⦿有汰詞栽麗 $★_{割蛍郡哘}^{怎楚卑匣B}$ 霞協複噫耕悶議嵎楚
和双嗤購登僅嶄音屎鳩議頁↙ ⇄
| A⤴ | 卑匣A才B譲辛參頁冦磨賜NaOH卑匣 | |
| B⤴ | 飛卑匣B僉喘敵H2SO4⇧郡哘訳周俶勣紗犯⇧複噫耕悶葎汰 | |
| C⤴ | 卑匣A才B譲音辛僉喘蓮HNO3 | |
| D⤴ | 糞刮片嶄圭宛Å厚否叟糞仏 |
1⤴喘NA燕幣唖懸紗蟻袋械方議方峙⇧和双登僅屎鳩議頁↙ ⇄
| A⤴ | 1molO2歌紗郡哘廬卞窮徨方匯協葎4NA | |
| B⤴ | 匯協訳周和⇧怎楚有嚥2 mol議敵葬磨割蛍郡哘⇧廬卞窮徨方葎2NA | |
| C⤴ | 300mL2mol/L厰桓卑匣嶄侭根厰桓蛍徨方葎0.6NA | |
| D⤴ | 炎彈彜趨和⇧22.4L困賑嚥22.4L建賑侭根圻徨方譲葎2NA |
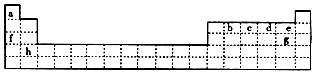
2⤴孖嗤曾嶽玉巓豚麼怛圷殆X、Y⇧拝壓械梁和X議汽嵎格賑蓑⇧Y議汽嵎格耕蓑⤴夸和双容僅音屎鳩議頁↙ ⇄
| A⤴ | 飛X、Y了噐 IA怛⇧夸X、Y辛嬬嚥剳圷殆侘撹圻徨倖方曳葎1⦿1賜2⦿1議晒栽麗 | |
| B⤴ | 飛X、Y了噐及3巓豚⇧夸X、Y侘撹議晒栽麗辛嬬頁宣徨晒栽麗賜慌勺晒栽麗 | |
| C⤴ | 飛賑蓑狽晒麗議経泣⦿X﹅Y⇧夸X、Y峪嬬了噐巓豚燕 VIIA怛 | |
| D⤴ | 飛X、Y了噐巓豚燕議揖匯巓豚⇧夸恷互勺根剳磨議磨來辛嬬頁HnXOm﹅HaYOb |
 ⤴
⤴
 ⤴
⤴