题目内容
14.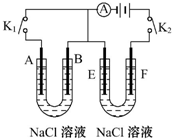 如图所示,A、F为石墨电极,B、E为铁片电极.按要求回答下列问题.
如图所示,A、F为石墨电极,B、E为铁片电极.按要求回答下列问题.(1)打开K2,合并K1.B为负极,A的电极反应为O2+4e-+2H2O═4OH-.
最终可观察到的现象是溶液中产生白色沉淀,然后变为灰绿色,最终变为红褐色.
涉及的化学反应方程式有:2Fe+O2+2H2O=2Fe(OH)2,Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(2)打开K1,合并K2.E为阴极,F极的电极反应为2Cl--2e-═Cl2↑,
检验F极产生气体的方法是用湿润的淀粉-KI试纸检验,试纸变蓝则说明是氯气.
(3)若往U形管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是AE.
分析 (1)当打开K2,闭合K1时,铁片、石墨和NaCl溶液构成原电池,负极为铁,石墨作正极,发生吸氧腐蚀;
(2)当打开K1,闭合K2时,铁片、石墨和NaCl溶液构成电解池,说明作阳极,铁作阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,可以用湿润的淀粉碘化钾试纸检验氯气;
(3)进行(1)时,正极附近生成氢氧根离子,进行(2)时,阴极附近生成氢氧根离子,酚酞试液遇碱变红色.
解答 解:(1)当打开K2,闭合K1时,铁片、石墨和NaCl溶液构成原电池,负极为铁,电极反应式为:Fe-2e-═Fe2+,正极为石墨,正极的电极反应式为:O2+4e-+2H2O═4OH-,由于Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+O2+2H2O═4Fe(OH)3,所以可观察到的现象是:溶液中产生白色沉淀,然后变为灰绿色,最终变为红褐色,最终的现象为溶液中有红褐色沉淀生成;发生的反应方程式为:2Fe+O2+2H2O=2Fe(OH)2,Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+O2+2H2O═4Fe(OH)3;
故答案为:负;O2+4e-+2H2O═4OH-;溶液中有红褐色沉淀生成;2Fe+O2+2H2O=2Fe(OH)2,Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(2)当打开K1,闭合K2时,铁片、石墨和NaCl溶液构成电解池,阴极为铁,电极反应式为:2H++2e-═H2↑,阳极为石墨,电极反应式为:2Cl--2e-═Cl2↑,检验Cl2的方法是:用湿润的淀粉-KI试纸检验,试纸变蓝则说明是氯气,
故答案为:阴;2Cl--2e-═Cl2↑;用湿润的淀粉-KI试纸检验,试纸变蓝则说明是氯气;
(3)由于A极O2得到电子产生OH-,E极上水放电产生H2和OH-,均导致电极区域呈碱性,所以A、E电极周围遇酚酞变红,
故答案为:AE.
点评 本题考查了原电池和电解池原理,正确判断原电池和电解池是解本题关键,难点是电极反应式的书写,知道氯气的检验方法,难度中等,侧重于考查学生的分析能力和对基础知识的应用能力.

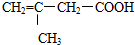 的结构,它不可能发生的反应是( )
的结构,它不可能发生的反应是( )| A. | 与银氨溶液反应析出银 | |
| B. | 使溴的四氯化碳溶液褪色 | |
| C. | 与乙醇在浓硫酸催化下发生酯化反应 | |
| D. | 与新制氢氧化铜反应 |
(1)下列有关滴定操作的顺序正确的是B
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④B.③⑤①②④C.③⑤②①④D.②①③⑤④
(2)用标准的盐酸滴定待测的NaOH溶液时,一手握酸式滴定管的活塞,一手摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,本实验滴定达到终点的标志是溶液颜色由黄色突变为橙色,且半分钟内不变色
(3)下列哪些操作会使测定结果偏高ABC
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后未用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数仰视滴定管读数,滴定后俯视滴定管读数
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0mol•L-1盐酸的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 20.00 | 0.00 | 22.20 |
| 第二次 | 20.00 | 1.56 | 25.50 |
| 第三次 | 20.00 | 0.22 | 22.48 |
| A. | NH3、O2、HCl | B. | N2、H2、HCl | C. | CO2、NO、O2 | D. | H2S、O2、SO2 |
(1)N、Al、Si、Zn、Fe五种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | … |
| Im/kJ•mol-1 | 578 | 1817 | 2745 | 11578 | … |
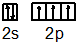 .
.(2)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为15NA;
(3)K3[Fe(CN)6]可用来检验Fe2+,向硫酸亚铁溶液中加入几滴K3[Fe(CN)6],观察到的现象是产生蓝色沉淀,与CN-互为等电子体的微粒有CO、N2等(填化学式,写2种)
C、N、O三种元素第一电离能由大到小的顺序为N>O>C;三种元素形成的简单氢化物分子中键角由大到小依次为CH4>NH3>H2O(用分子式表示).
(4)已知Fe的相对原子质量为M,阿佛加德罗常数用NA表示,已知金属Fe为体心立方堆积,若Fe原子半径为acm,密度为ρg/cm3.则M=$\frac{32ρ{a}^{3}{N}_{A}}{3\sqrt{3}}$(用ρ、a、NA表达式表示)
| A. | 合金的熔点一般比组分金属高 | B. | 合金中只含金属元素 | ||
| C. | 合金的机械性能一般比组分金属好 | D. | 合金的硬度一般比组分小 |
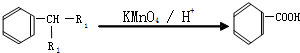
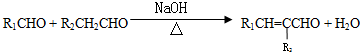 (-R1、R2表示氢原子或烃基)
(-R1、R2表示氢原子或烃基)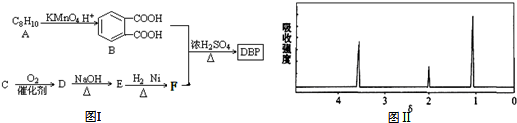
 ,该反应的反应类型为取代反应或酯化反应.
,该反应的反应类型为取代反应或酯化反应.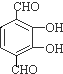 、
、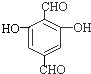 等.
等.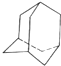 油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示: