题目内容
11.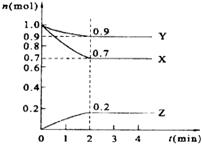 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示. (1)X的转化率是30%,
(2)由图中所给数据进行分析,该反应的化学方程式为3X+Y?2Z;
(3)反应从开始至2min末,v(Z)=0.05mol/(L•min),v(X)=0.075mol/(L•min),
(4)当反应进行到第2min,该反应是达到平衡状态,X所占的体积分数为38.9%.
分析 由图象可知,反应达到2min时达到平衡状态,各物质的物质的量不变,根据图知,该反应中参加反应的△n(X)=(1.0-0.7)mol=0.3mol、△n(Y)=(1.0-0.9)mol=0.1mol、△n(Z)=(0.2-0)mol=0.2mol,则X、Y、Z的计量数之比=0.3mol:0.1mol:0.2mol=3:1:2,以此可确定反应的化学方程式,并以此计算转化率、反应速率以及体积分数,以此解答该题.
解答 解:(1)2min时C的物质的量由1mol变化为0.7mol,则转化率为$\frac{1.0mol-0.7mol}{1.0mol}×100%$=30%,故答案为:30%;
(2)同一可逆反应同一时间段内参加反应的各物质的物质的量之比等于其计量数之比,根据图知,该反应中参加反应的△n(X)=(1.0-0.7)mol=0.3mol、△n(Y)=(1.0-0.9)mol=0.1mol、△n(Z)=(0.2-0)mol=0.2mol,则X、Y、Z的计量数之比=0.3mol:0.1mol:0.2mol=3:1:2,则该反应方程式为3X+Y?2Z,
故答案为:3X+Y?2Z;
(3)反应从开始至2min末,v(Z)=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L•min),v(X)=$\frac{\frac{0.3mol}{2L}}{2min}$=0.075mol/(L•min),故答案为:0.05mol/(L•min);0.075mol/(L•min);
(4)由图象可知反应达到2min时达到平衡状态,X所占的体积分数为$\frac{0.7}{0.9+0.7+0.2}×100%$=38.9%,故答案为:2;38.9%.
点评 本题考查化学平衡有关计算,为高频考点,侧重考查学生分析计算能力,明确平衡状态图象特点、各个物理量之间的关系是解本题关键,题目难度不大.

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案| A. | 质量 | B. | 原子数 | C. | 质子数 | D. | 密度 |
| A. | 被测样品中含有加热不挥发的杂质 | B. | 被测样品中含有加热易挥发的杂质 | ||
| C. | 实验前被测样品已有部分失水 | D. | 加热前所用的坩埚未完全干燥 |
 高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性.
高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性.(1)已知:4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑.K2FeO4在处理水的过程中所起的作用有杀菌消毒、吸附悬浮物.同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH=11.50的溶液.
(2)高铁酸钾有以下几种常见制备方法:
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 电解法 | 制备中间产物Na2FeO4,再与KOH溶液反应 |
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:2FeO42-+Fe3++8OH-=3FeO43-+4H2O.
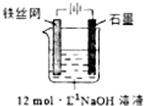
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应式为Fe+8OH--6e-═FeO42-+4H2O.
(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:3Zn+2K2FeO4+8H2O $?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,放电时负极材料为Zn,正极反应为:FeO42-+4H2O+3e-═Fe(OH)3+5OH-;.
(4)25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000L,含有2.0×l0-4mol•L-lK2FeO4的废水中的c(FeO42-)有沉淀产生,理论上至少加入Ca(OH)2的物质的量为2.27×10-2mol.
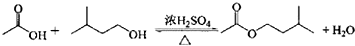
| 相对原子质量 | 密度/(g.cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.813 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊醇 | 130 | 0.8670 | 142 | 难溶 |
在A中加入4.4g异戊醇、6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热A,回流50min.反应液冷至室温后倒入分液漏斗中,分别用少最水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊脂3.9g.
回答下列问题:
(1)仪器B的名称是球形冷凝管.
(2)在洗涤操作中,第一次水洗的主要目的是洗掉大部分硫酸和醋酸;洗掉碳酸氢钠.
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后(填标号〕d.
a、直接将乙酸异戊酯从分液漏斗的上口倒出
b、直接将乙酸异戊从分液端斗的下口放出
c、先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d、先将水层从分液漏斗的下口放出,再将乙酸异戊酚从上口倒出
(4)本实验中加入过量乙酸的目的是提高醇的转化率.
(5)实验中加入少量无水MgSO4的目的是干燥乙酸异戊酯.
(6)在蒸馏操作中,仪器选择及安装都正确的是图2中的b(填标号).
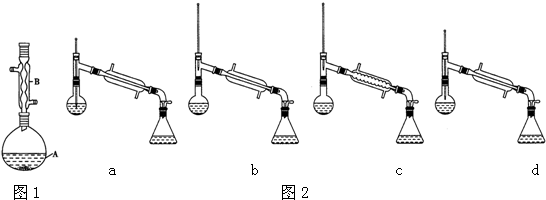
(7)本实验的产率是c(填标号).
a.30% b.40% c、60% d、90%
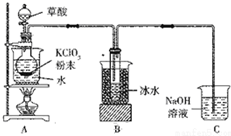 二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如图所示:
二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如图所示: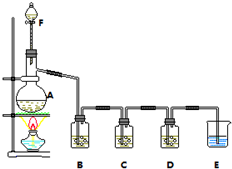 某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.