题目内容
16.有一真空密闭容器中,盛有amolPCl5,加热到200℃时,发生如下反应PCl5(g)?PCl3(g)+Cl2(g),反应达平衡时,PCl5所占体积分数为M%,若在同一温度下,同一容器中,最初投入2amolPCl5反应达平衡时,PCl5所占体积分数为N%,则M与N的关系正确的是( )| A. | M<N | B. | 2M=N | C. | N<M | D. | M=N |
分析 开始加入2molPCl5所到达的平衡,等效为开始加入1molPCl5到达平衡的基础上再通入1molPCl5,进一步等效为在开始加入1molPCl5到达平衡的基础上压强增大一倍,增大压强平衡向气体体积减小的方向移动.
解答 解:开始加入2molPCl5所到达的平衡,等效为开始加入1molPCl5到达平衡的基础上再通入1molPCl5,进一步等效为在开始加入1molPCl5到达平衡的基础上压强增大一倍,正反应为气体体积增大的反应,增大压强后与原平衡相比,平衡逆向移动,则平衡时的PCl5含量增大,即M<N,
故选:A.
点评 本题考查化学平衡影响因素,关键是构建平衡建立的途径,注意等效思想在化学平衡中应用.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
7.如果a克某气体中含有的分子数为b,则c克该气体的物质的量是(NA表示阿伏加德罗常数)( )
| A. | $\frac{bc}{a{N}_{A}}$ | B. | $\frac{ac}{b{N}_{A}}$ | C. | $\frac{ab}{c{N}_{A}}$ | D. | $\frac{b}{ac{N}_{A}}$ |
11.氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应生成H2和NaOH.下列叙述中,不正确的是( )
| A. | NaH的电子式为Na+[:H]- | |
| B. | NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同 | |
| C. | 微粒半径H-<Li+ | |
| D. | NaH与H2O反应时,水作氧化剂 |
1.用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | lmol Na2O2晶体中共含有2NA个离子 | |
| B. | 0.1 molAlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 | |
| C. | 常温常压下16gO2和O3混合气体含有NA个氧原子 | |
| D. | 电解精炼铜时每转移NA个电子,阳极生成氧气 |
8.下列说法中正确的是( )
| A. | 含H+的溶液一定呈酸性 | |
| B. | pH=7的溶液一定呈中性 | |
| C. | c(OH-)═c(H+)的溶液一定呈中性 | |
| D. | 水中加入硫酸恢复至室温后,Kw=c(H+)•c(OH-)将变大 |
5.结合下图判断,下列叙述正确的是( )
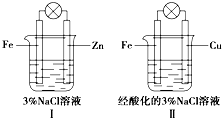

| A. | Ⅰ和Ⅱ中正极均被保护 | |
| B. | Ⅰ和Ⅱ中负极反应均是Fe-2e-═Fe2+ | |
| C. | Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-═4OH- | |
| D. | Ⅰ和Ⅱ中灯泡均会发亮 |
6.下列说法正确的是( )
| A. | 化合物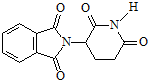 的分子式为C13H9O4N2 的分子式为C13H9O4N2 | |
| B. | 在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH | |
| C. | 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应 | |
| D. | 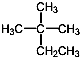 的系统命名为2-甲基-2-乙基丙烷 的系统命名为2-甲基-2-乙基丙烷 |
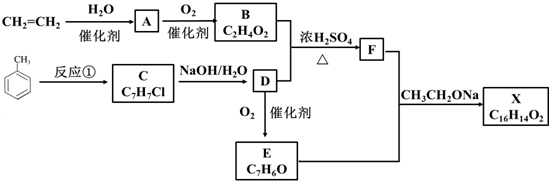
 .
. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O.
+2H2O. .
.