题目内容
(10分)某化学兴趣小组进行如下图所示的电化学实验,实验前查资料获知:铁氰化钾
(K3[Fe(CN)6])遇Fe2+产生 蓝色沉淀。V形管以多孔Pt为电极;U形管A端滴入1~2滴K3[Fe(CN)6]溶液。

(1)开始时,接通K电键:U形管中无沉淀,可知电源正极为 (填“a”或“b”).Fe电极上发生的电极反应为 。
(2)断开K电键,V形管中为将 能转化为 能的装置;U形管A端现象为 。
(1)b;2H++2e-=H2↑(2)电能;化学能;产生蓝色沉淀。
【解析】
试题分析:(1)开始时,接通K电键:U形管中无沉淀,说明溶液中为生成亚铁离子,则铁为电解池的阴极,则电源的正极为b;铁为阴极,电极反应为:2H++2e-=H2↑;(2)断开K电键,左侧形成原电池,V形管中为电解池,是将电能转化为化学能,铁为原电池的负极,失去电子变成亚铁离子,铁氰化钾(K3[Fe(CN)6])遇Fe2+产生蓝色沉淀。
考点:原电池和电解池的原理。

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
 2P(g);△H<0。若起始温度相同分别向三个容器中通入3molM和1mol N,则达到平衡时各容器中P物质的体积分数由大到小的顺序为
2P(g);△H<0。若起始温度相同分别向三个容器中通入3molM和1mol N,则达到平衡时各容器中P物质的体积分数由大到小的顺序为
 、②
、②  两种溶液的叙述不正确的是
两种溶液的叙述不正确的是 ) ②<①
) ②<① 
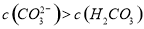
 B.
B.
 D.
D.