题目内容
11.生活处处有化学,下列说法正确的是( )| A. | 棉花与淀粉互为同分异构体 | |
| B. | 豆浆煮沸后,蛋白质变成了氨基酸 | |
| C. | 纤维素与蛋白质都是天然高分子化合物 | |
| D. | 油脂在酸性条件下可水解为高级脂肪酸盐和甘油 |
分析 A.棉花的主要成分为纤维素,纤维素与淀粉分子式不同;
B.豆浆煮沸过程中,蛋白质没有发生水解;
C.根据高分子化合物的定义判断;
D.油脂在酸性条件下可水解为高级脂肪酸和甘油.
解答 解:A.棉花的主要成分为纤维素,纤维素与淀粉都是高分子化合物,聚合度不同,则分子式不同,不是同分异构体,故A错误;
B.豆浆煮沸过程中,蛋白质没有发生水解,故B错误;
C.高分子化合物的相对分子质量在10000以上,多为高聚物,则纤维素与蛋白质都是天然高分子化合物,故C正确;
D.油脂在酸性条件下可水解为高级脂肪酸和甘油,碱性条件下可水解生成高级脂肪酸盐,故D错误.
故选C.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握常见有机物的组成和性质,注意同分异构体以及高分子化合物的定义,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.甲氯芬那酸是一种非甾体抗炎镇痛药,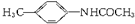 是制备甲氯芬那酸的中间产物,该中间产物是利用下面的反应制得:
是制备甲氯芬那酸的中间产物,该中间产物是利用下面的反应制得: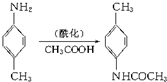 则该反应的反应类型为( )
则该反应的反应类型为( )
 是制备甲氯芬那酸的中间产物,该中间产物是利用下面的反应制得:
是制备甲氯芬那酸的中间产物,该中间产物是利用下面的反应制得: 则该反应的反应类型为( )
则该反应的反应类型为( )| A. | 酯化反应 | B. | 加成反应 | C. | 消去反应 | D. | 取代反应 |
2.下列实验设计的步骤及现象均正确的是( )
| 实验目的 | 实 验 步 骤 及 现 象 | |
| A | 证明氯水有酸性 | 试样$\stackrel{滴加紫色石蕊}{→}$溶液变红色,且长时间不变 |
| B | 检验某红棕色气体是否溴蒸汽 | 试样$\stackrel{滴入淀粉KI溶液}{→}$观察溶液是否变蓝 |
| C | 证明酸性条件 H2O2氧化性比I2强 | NaI溶液$\stackrel{加入30%H_{2}O_{2}溶液}{→}$$\stackrel{加入稀硝酸及淀粉}{→}$溶液变蓝色 |
| D | 提纯含有少量乙酸的乙酸乙酯 | 试样$\stackrel{加入过量饱和Na_{2}CO_{3}溶液}{→}$$\stackrel{静置分液}{→}$较纯净乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
19.如表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
试回答下列问题:
(1)请写出元素N的基态原子电子排布式1s22s22p63s23p63d74s2或[Ar]3d74s2.
(2)元素B、G形成的单质熔点更高的是Li(填化学式),原因是Li和Na的价电子数相同,但Li原子半径小于Na原子半径,所以Li金属键更强,熔点更高.
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是非极性(填“极性”或“非极性”)分子.
(4)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有①③(填序号),CS2分子的空间构型是直线型.
(5)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为[Co(NH3)5SO4]Br.
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | K | L | ||||||||||||
| M | N | ||||||||||||||||
(1)请写出元素N的基态原子电子排布式1s22s22p63s23p63d74s2或[Ar]3d74s2.
(2)元素B、G形成的单质熔点更高的是Li(填化学式),原因是Li和Na的价电子数相同,但Li原子半径小于Na原子半径,所以Li金属键更强,熔点更高.
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是非极性(填“极性”或“非极性”)分子.
(4)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有①③(填序号),CS2分子的空间构型是直线型.
(5)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为[Co(NH3)5SO4]Br.
16.决定物质性质的重要因素是物质结构.请回答下列问题.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
A通常显+3价,B元素的核外电子排布式为1s22s22p63s2.
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2和sp3.
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),已知3种离子晶体的晶格能数据如下表:
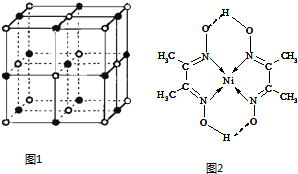
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是TiN>MgO>CaO>KCl.
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个.
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.FeCl3和CuCl2中,适合作录音带磁粉原料的是FeCl3.
(5)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A.离子键 B.极性键 C.金属键
D.配位键 E.氢键 F.非极性键.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2和sp3.
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |

| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个.
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.FeCl3和CuCl2中,适合作录音带磁粉原料的是FeCl3.
(5)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A.离子键 B.极性键 C.金属键
D.配位键 E.氢键 F.非极性键.
3.下列有机物相应说法正确的是( )
| A. | 乙烷中混有乙烯,提纯方法:催化剂条件下与氢气混合反应 | |
| B. | 乙酸乙酯中混有乙酸,提纯方法:用过量饱和碳酸钠溶液洗涤后分液 | |
| C. | 乙醇中混有乙酸,验证乙酸存在的方法:加金属钠,看是否有气泡 | |
| D. | 蔗糖水解产物的验证:在冷却后的水解液中直接加入银氨溶液,水浴加热,看是否有银镜产生 |
20.化学与社会、生产和生活密切相关.对下列现象或事实的解释正确是( )
| 选项 | 现象或事实 | 解释 |
| A | 配制FeCl3溶液时,加入适量盐酸 | 增大Cl-浓度,可以抑制Fe3+水解 |
| B | Cl2通入人品红溶液中,品红褪色 | Cl2具有漂白性 |
| C | 久置的漂白粉质量减小 | 漂白粉中的Ca(ClO)2转化为CaCO3 |
| D | AgI可用于人工降雨 | AgI气化时吸热 |
| A. | A | B. | B | C. | C | D. | D |
1.下列有关说法正确的是( )
| A. | 海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 | |
| B. | 锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去 | |
| C. | 日本福岛核电站爆炸时释放的两种放射性核素131I与137Cs(铯)的中子数相等 | |
| D. | 铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝 |
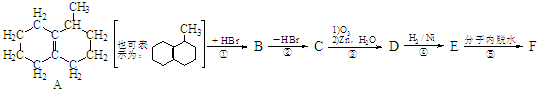
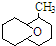 )外,还得到它的同分异构体,其中B、C、D、E、F、分别代表一种或多种物质.已知:
)外,还得到它的同分异构体,其中B、C、D、E、F、分别代表一种或多种物质.已知: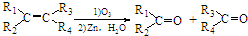 (R1,R2,R3,R4为烃基或H)
(R1,R2,R3,R4为烃基或H)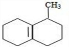 .
.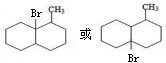 ;
; .
.