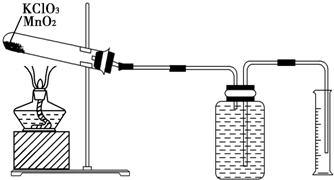
��Ŀ����
12������һ��ͭ�����Ļ������Ʒ��ijѧ��ȡ10.0g����Ʒ�����ձ��У���80.0mLϡ������Ĵμ����ձ�������ؼ�¼���й����ݼ�¼�����
| ������Ĵ������ | ������������/mL | ʣ����������/g |
| 1 | 20.0 | 7.20 |
| 2 | 20.0 | 4.40 |
| 3 | 20.0 | 2.00 |
| 4 | 20.0 | 2.00 |
��2�����������������Һ����������ʵ���Ũ�ȣ�
���� ��1������ϡ���ᷴӦ��������������������
��2�������������ݿ�֪��ǰ������������㣬�õ�һ�����ݼ��㣬��1���вμӷ�Ӧ��FeΪ10g-7.20g=2.80g��������ȫ��Ӧ�����ݷ���ʽ����20mL��Һ����������ʵ������ٸ���c=$\frac{n}{V}$���㣮
��� �⣺��1������ϡ���ᷴӦ����������������������Ӧ���ӷ���ʽΪ��Fe+2H+=Fe2++H2����
�ʴ�Ϊ��Fe+2H+=Fe2++H2����
��2���Ƚϱ��������ݿ��Է��֣�ÿ����20mL���ᣬ��1��2��ʣ��������������С2.8g�ˣ�����3�μ���2.4g����ǰ������������㣬�õ�һ�����ݼ��㣬��1���вμӷ�Ӧ��FeΪ��10g-7.20g=2.80g��
Fe+H2SO4=FeSO4+H2��
56g 1mol
2.8g n
n=$\frac{2.8g��1mol}{56g}$=0.05mol
����������ʵ���Ũ��Ϊ��$\frac{0.05mol}{0.02L}$=2.5mol/L��
�𣺸���������ʵ���Ũ��Ϊ2.5mol/L��
���� ���⿼�黯ѧ����ʽ���йؼ��㣬��Ŀ�Ѷ��еȣ����ؿ���ѧ����ʵ�����ݵķ����������������ݹ��������仯�жϹ������ǽ���ؼ�������������ѧ���Ļ�ѧ����������

��ϰ��ϵ�д�
�����Ŀ
1��������Ԫ���У�����������Ԫ�ص��ǣ�������
| A�� | �� | B�� | �� | C�� | �� | D�� | �� |
7������ͼʾ���Ӧ������������ǣ�������


| A�� | ͼ1��ʾ��ͬ�¶���pH=1������ʹ�����Һ�ֱ��ˮϡ��ʱpH�ı仯���ߣ��������ߢ�Ϊ���ᣬ��b����Һ�ĵ����Ա�a��ǿ | |
| B�� | ͼ2�д�ˮ�������¶ȣ��Ϳ��Դ�a��䵽c�� | |
| C�� | ͼ1�У�b�������Ũ�ȴ���a�������Ũ�� | |
| D�� | ͼ2����b���Ӧ�¶��£���pH=2��H2SO4��pH=10��NaOH��Һ�������Ϻ���Һ������ |
17�������йػ�ѧ������ȷ���ǣ�������
| A�� | ��ϩ�Ľṹ��ʽCH2CH2 | B�� | �Ҵ��ķ���ʽC2H6O | ||
| C�� | ������֬�Ľṹ��ʽ��CH3COOC2H5 | D�� | ���Ȼ�̼�ĵ���ʽ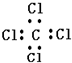 |
4���ö��Ե缫���������Һ��һ��ʱ����ټ���һ����������һ�����ʣ��������ڣ�����Һ����ԭ����Һ��ȫһ�����ǣ�������
| A�� | HCl[H2O] | B�� | NaOH[Na2O] | C�� | KI[HI] | D�� | CuSO4[Cu��OH��2] |
1�����и����л�����۰����ֱ�����ϣ�ֻҪ������һ������ȫȼ�պ�����CO2����������ͬ���ǣ�������
| A�� | ���顢��Ȳ | B�� | ��ȩ������ | C�� | �Ҵ����Ҷ��� | D�� | �ױ������� |
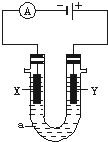 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺