题目内容
14.某粒子用${\;}_Z^A{X^{n-}}$表示,下列关于该粒子的叙述错误的是( )| A. | 质子数=A-n | B. | 中子数=A-Z | C. | 电子数=Z+n | D. | 所带电荷数=n |
分析 元素符号的左下角表示质子数,左上角表示质量数,中子数=质量数-质子数,核电荷数=质子数=原子序数.阴离子中核外电子数=质子数+电荷数,据此分析解答.
解答 解:AZXn-中质子数为Z,质量数为A,中子数=质量数-质子数=A-Z,核电荷数=Z,所带的电荷为n-,所带电荷数=n,该微粒是阴离子,所以核外电子数=质子数+电荷数=Z+n.
A.所含的质子数为Z,故A错误;
B.所含的中子数为A-Z,故B正确;
C.所含的电子数为Z+n,故C正确;
D.所带的电荷为n-,所带电荷数=n,故D正确;
故选A.
点评 本题考查了质子数、质量数、中子数、核外电子数之间的关系,题目难度不大,明确各物理量之间的关系是解本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列说法不正确的是( )
| A. | 氢能将是二十一世纪的重要能源,推广应用氢能最关键技术是高容量储氢材料的研制 | |
| B. | 纳米TiO2光触媒技术制成的“木地板精油”能将水气转化为活性氧,由此可推测TiO2光触媒技术制成的“木地板精油可以有效降解甲醛、苯、氨等居室污染物 | |
| C. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强酸、强碱都会“断路” | |
| D. | 门捷列夫提出的元素周期律为发现新元素、合成新材料提供了新思路 |
9.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 密封保存的46 g NO2气体含有分子数小于NA | |
| B. | 标准状况下,22.4 LCCl4中含有的氯原子数目为4NA | |
| C. | 18gT2O(3H2O)中,含有的电子总数为10NA | |
| D. | 含NA个Na+的Na2O2溶于1 L水中,Na+的物质的量浓度为1 mol/L |
19.下列叙述正确的是( )
| A. | 非金属原子间以共价键结合的物质都是共价化合物 | |
| B. | 金属元素和非金属元素不可能形成共价化合物 | |
| C. | 凡是能电离出离子的化合物都是离子化合物 | |
| D. | 离子化合物中可能有共价键 |
6.下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,原子半径最大的是Na,其离子的原子结构示意图为
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH;
(3)按要求写出下列两种物质的电子式:①的氢化物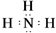 ;⑨的最高价氧化物的对应的水化物的电子式
;⑨的最高价氧化物的对应的水化物的电子式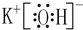 ;
;
(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):Cl2+2NaBr=2NaCl+Br2.
(5)请用电子式表示④和⑦形成的化合物的形成过程 .
.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH;
(3)按要求写出下列两种物质的电子式:①的氢化物
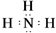 ;⑨的最高价氧化物的对应的水化物的电子式
;⑨的最高价氧化物的对应的水化物的电子式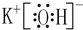 ;
;(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):Cl2+2NaBr=2NaCl+Br2.
(5)请用电子式表示④和⑦形成的化合物的形成过程
 .
.
4.在三个体积为1L、温度保持不变的容器中,分别发生反应3A(g)+B(g)?3C(g),5min后各容器反应达平衡状态,其中甲容器中A的物质的量为2.4mol,下列说法正确的是( )
| 反应前各物质的物质的量/mol | |||
| A | B | C | |
| 甲 | 6 | 2 | 0 |
| 乙 | 0 | 0 | 6 |
| 丙 | 6 | 2 | 6 |
| A. | 带大平衡时,丙中A的溶度是甲中的2倍 | |
| B. | 若反应开始时向容器中加入A为2mol,B为0.5mol,C为3mol,则反应v(正)>v(逆) | |
| C. | 到达平衡时,甲中A的转化率等于乙中C的转化率 | |
| D. | 若保持恒温恒压,达到平衡后再向乙容器中再充入2molC,C的百分含量不变 |