题目内容
2.已知:A(g)+2B(g)?C(g)+D(g)△H<0,一定温度下,2molA和2molB在2L密闭容器中反应,10min后达到平衡,此时容器压强降为原来的$\frac{4}{5}$,下列叙述正确的是( )| A. | 从开始到平衡,A的反应速率为0.08mol•L-1•min-1 | |
| B. | 随着反应的进行,混合气体的密度逐渐减小 | |
| C. | 达到平衡时,B的转化率为20% | |
| D. | 该温度下,反应的平衡常数K=$\frac{20}{3}$ |
分析 已知:A(g)+2B(g)?C(g)+D(g)△H<0,一定温度下,2molA和2molB在2L密闭容器中反应,10min后达到平衡,结合化学三行计算得到,设A消耗物质的量为x,
A(g)+2B(g)?C(g)+D(g)
起始量(mol) 2 2 0 0
变化量(mol) x 2x x x
平衡量(mol)2-x 2-2x x x
此时容器压强降为原来的$\frac{4}{5}$,气体物质的量之比等于气体压强之比,
2-x+2-2x+x+x=$\frac{4}{5}$×(2+2)
x=0.8mol,
A.反应速率v=$\frac{△c}{△t}$=;
B.反应前后气体体积不变,气体质量不变,密度ρ=$\frac{m}{V}$;
C.转化率=$\frac{消耗量}{起始量}$×100%;
D.平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积.
解答 解:已知:A(g)+2B(g)?C(g)+D(g)△H<0,一定温度下,2molA和2molB在2L密闭容器中反应,10min后达到平衡,结合化学三行计算得到,设A消耗物质的量为x,
A(g)+2B(g)?C(g)+D(g)
起始量(mol) 2 2 0 0
变化量(mol) x 2x x x
平衡量(mol)2-x 2-2x x x
此时容器压强降为原来的$\frac{4}{5}$,气体物质的量之比等于气体压强之比,
2-x+2-2x+x+x=$\frac{4}{5}$×(2+2)
x=0.8mol,
A.从开始到平衡,A的反应速率v=$\frac{△c}{△t}$=$\frac{\frac{0.8mol}{2L}}{10min}$=0.04mol•L-1•min-1,故A错误;
B.反应前后气体体积不变,气体质量不变,密度ρ=$\frac{m}{V}$,随着反应的进行,混合气体的密度始终不变,故B错误;
C.达到平衡时,B的转化率=$\frac{消耗量}{起始量}$×100%=$\frac{2×0.8mol}{2}$×100%=80%,故C错误;
D.K=$\frac{\frac{0.8}{2}×\frac{0.8}{2}}{\frac{2-0.8}{2}×(\frac{2-2×0.8}{2})^{2}}$=$\frac{20}{3}$,故D正确;
故选D.
点评 本题考查了化学平衡的计算,题目难度中等,明确气体压强之比等于气体物质的量之比为解答关键,注意掌握三段式在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.

 名校课堂系列答案
名校课堂系列答案| A. | 若a≥2b,发生的反应化学方程式为:2C2H2+O2═4C+2H2O | |
| B. | 若($\frac{2}{5}$)b<a<($\frac{2}{3}$)b,燃烧后在密闭容器中加入含amolCa(OH)2的石灰水,发生反应的离子方程式为:OH-+CO2═HCO3- | |
| C. | 若a<($\frac{2}{5}$)b,燃烧过程中转移的电子的物质的量为10amol | |
| D. | 若a=($\frac{1}{2}$)b,燃烧产物既有CO2又有CO,且n(CO2):n(CO)=1 |
| A. | 金刚石和石墨互为同素异形体,熔点和硬度都很高 | |
| B. | 氕、氘、氚是氢元素的三种核素,质子数都是1 | |
| C. | 乙醇和二甲醚(CH3-O-CH3)互为同系物 | |
| D. | C4H10的一氯代物只有一种 |
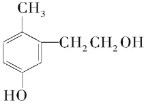
| A. | 它是苯酚的同系物 | |
| B. | 1 mol该物质能与溴水反应消耗2molBr2发生取代反应 | |
| C. | 1 mol该有机物能与足量金属钠反应生成0.5mol H2 | |
| D. | 1 mol该有机物能与2molNaOH反应 | |
| E. | 该物质在加热条件下可以与铜反应生成一种具有醛基的化合物 |
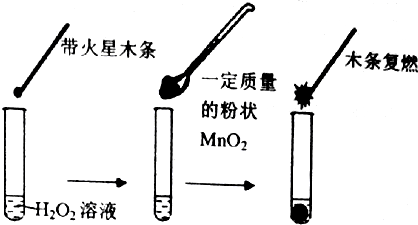
(1)甲同学欲用图所示实验来证明MnO2是H2O2分解反应的催化剂. 该实验不能 (填“能”或“不能”)达到目的,原因是因为没有确认MnO2的质量和性质是否改变.(若能,不必回答原因)
(2)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10mL5%H2O2)
| 试管 | Ⅰ | Ⅱ | Ⅲ |
| 滴加试剂 | 5滴0.1mol•L-1FeCl3 | 5滴0.1mol•L-1 CuCl2 | 5滴0.3mol•L-1 NaCl |
| 产生气泡情况 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无气泡产生 |
(3)在上述实验过程中,分别检测出溶液中有二价铁生成,查阅资料得知:将作为催化剂的FeCl3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的化学方程式分别是2FeCl3+H2O2=2FeCl2+O2↑+2HCl和2FeCl2+H2O2+2HCl=2FeCl3+2H2O(按反应发生的顺序写).
| A. | 豆类、糙米、谷物 | B. | 胡萝卜、水果、猪肝 | ||
| C. | 肉、蛋、奶 | D. | 新鲜蔬菜、黄玉米、黄豆 |
| A. | Fe和醋酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 大理石和稀盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | FeCl2溶液与Cl2的反应:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | Cl2与H2O反应:Cl2+H2O═2H++Cl-+ClO- |