题目内容
我校化学兴趣小组拟通过中和滴定实验验证某品牌陈醋的酸度.
(1)查阅资料:
①食醋组成极为复杂,除水以外的主要成分是醋酸CH3COOH,此外还有其他各种有机物和一些无机物等微量成分,醋酸的含量远远多于其他成分的含量.另外其中含一些色素成分,使食醋呈棕色(白醋除外).
②0.1mol/L醋酸与氢氧化钠反应的滴定终点的pH约为
A 5.6 B 7.0 C 8.8 D 13.0
③包装显示该陈醋的酸度约是3.6g/100mL
(2)由以上资料,同学们认为:
①测量时可以忽略老陈醋其他成分特别是有机酸所带来的影响.
②根据陈醋的特点,只能选用 来指示滴定终点.
A 甲基橙 B 酚酞 C 石蕊 D pH计
③为使滴定时溶液中的醋酸浓度接近0.1mol/L,应将10ml样品醋稀释至 .
A 36ml B 60ml C 360ml D 600ml
(3)配制标准氢氧化钠溶液
由于NaOH在称量过程中极易吸水,配好的溶液浓度往往比预期偏小.故实验小组先用0.1010mol/L 的KHP标准溶液准确测定NaOH溶液的浓度(KHP与NaOH按物质的量比1:1完全反应).向锥形瓶中盛入20.00ml NaOH溶液时,应用 量取.
A.20ml 的量筒 B.100ml 的容量瓶 C.碱式滴定管 D.酸式滴定管
(4)用标准氢氧化钠溶液测定醋酸的浓度,并换算为酸度.
计算得出该陈醋样品的酸度为 g/100mL.(计算结果保留4为有效数字)
(1)查阅资料:
①食醋组成极为复杂,除水以外的主要成分是醋酸CH3COOH,此外还有其他各种有机物和一些无机物等微量成分,醋酸的含量远远多于其他成分的含量.另外其中含一些色素成分,使食醋呈棕色(白醋除外).
②0.1mol/L醋酸与氢氧化钠反应的滴定终点的pH约为
A 5.6 B 7.0 C 8.8 D 13.0
③包装显示该陈醋的酸度约是3.6g/100mL
(2)由以上资料,同学们认为:
①测量时可以忽略老陈醋其他成分特别是有机酸所带来的影响.
②根据陈醋的特点,只能选用
A 甲基橙 B 酚酞 C 石蕊 D pH计
③为使滴定时溶液中的醋酸浓度接近0.1mol/L,应将10ml样品醋稀释至
A 36ml B 60ml C 360ml D 600ml
(3)配制标准氢氧化钠溶液
由于NaOH在称量过程中极易吸水,配好的溶液浓度往往比预期偏小.故实验小组先用0.1010mol/L 的KHP标准溶液准确测定NaOH溶液的浓度(KHP与NaOH按物质的量比1:1完全反应).向锥形瓶中盛入20.00ml NaOH溶液时,应用
A.20ml 的量筒 B.100ml 的容量瓶 C.碱式滴定管 D.酸式滴定管
| V(NaOH) | V(KHP)平均 |
| 20.00mL | 18.00mL |
| V(稀释后的醋) | V(NaOH)平均 |
| 18.00mL | 20.00mL |
考点:中和滴定
专题:实验题
分析:(1)醋酸与NaOH恰好反应生成醋酸钠,溶液显碱性,pH稍大于7;
(2)碱滴定酸,选择酚酞为指示剂,滴定终点时无色变为红色;的酸度约是3.6g/100mL,浓度为
=0.6mol/L,结合稀释前后溶质的物质的量不变计算;
(3)先用0.1010mol/L 的KHP标准溶液准确测定NaOH溶液的浓度,则NaOH盛放在锥形瓶中,选择碱式滴定管准确量取;
(4)结合n(醋酸)=n(NaOH)=n(KHP)计算.
(2)碱滴定酸,选择酚酞为指示剂,滴定终点时无色变为红色;的酸度约是3.6g/100mL,浓度为
| ||
| 0.1L |
(3)先用0.1010mol/L 的KHP标准溶液准确测定NaOH溶液的浓度,则NaOH盛放在锥形瓶中,选择碱式滴定管准确量取;
(4)结合n(醋酸)=n(NaOH)=n(KHP)计算.
解答:
解:(1)醋酸与NaOH恰好反应生成醋酸钠,溶液显碱性,pH稍大于7,只有pH=8.8符合,故答案为:C;
(2)碱滴定酸,选择酚酞为指示剂,滴定终点时无色变为红色,但另外其中含一些色素成分,干扰终点判断,则选择D中pH计指示滴定终点;酸度约是3.6g/100mL,浓度为
=0.6mol/L,由稀释前后溶质的物质的量不变可知,稀释后的体积为
=0.06L=60mL,
故答案为:D;B;
(3)先用0.1010mol/L 的KHP标准溶液准确测定NaOH溶液的浓度,则NaOH盛放在锥形瓶中,选择碱式滴定管准确量取,故答案为:C;
(4)由n(醋酸)=n(NaOH)=n(KHP)可知,c(醋酸)=
=0.101mol/L,该陈醋样品的酸度为3.6g/100mL×
=3.636g/100mL,
故答案为:3.636.
(2)碱滴定酸,选择酚酞为指示剂,滴定终点时无色变为红色,但另外其中含一些色素成分,干扰终点判断,则选择D中pH计指示滴定终点;酸度约是3.6g/100mL,浓度为
| ||
| 0.1L |
| 0.01L×0.6mol/L |
| 0.1mol/L |
故答案为:D;B;
(3)先用0.1010mol/L 的KHP标准溶液准确测定NaOH溶液的浓度,则NaOH盛放在锥形瓶中,选择碱式滴定管准确量取,故答案为:C;
(4)由n(醋酸)=n(NaOH)=n(KHP)可知,c(醋酸)=
| 0.101mol/L×0.018L |
| 0.018L |
| 0.101 |
| 0.1 |
故答案为:3.636.
点评:本题考查中和滴定,为高频考点,把握滴定原理、实验仪器及误差分析为解答的关键,注意(4)中计算为解答的难点,题目难度不大.

练习册系列答案
相关题目
充分利用已有的数据是解决化学问题方法的重要途径.对数据的利用情况正确的是( )
| A、利用化学平衡常数判断化学反应进行的快慢 |
| B、利用溶解度数据判断氧化还原反应发生的可能性 |
| C、利用沸点数据推测将一些液体混合物分离的可能性 |
| D、利用物质的摩尔质量判断相同状态下不同物质密度的大小 |
下列反应的离子方程式书写正确的是( )
| A、用醋酸溶液除水垢:CaCO3+2H+═Ca2++H2O+CO2↑ |
| B、向FeBr2溶液中通入足量Cl2:Fe3++2Br-+Cl2═Fe3++Br2+2Cl- |
| C、向Na[Al(OH)4]溶液中通入过量CO2:[Al(OH)4]-+CO2═Al(OH)3↓+HCO3- |
| D、向Ba(OH)2溶液滴加NaHSO4溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
下列说法正确的是( )
| A、制作航天服的聚酯纤维和用于制光缆的光导纤维都是新型无机非金属材料 |
| B、使用太阳能、风能等清洁能源能减少PM2.5的污染 |
| C、水泥、玻璃、水晶饰物都是硅酸盐制品 |
| D、用浸泡过溴的四氯化碳溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的 |
 CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是
CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是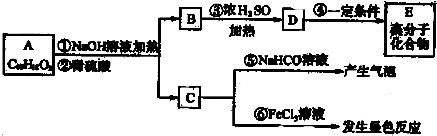
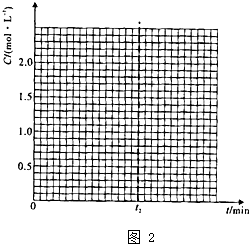
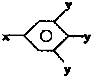 (其中-x、一y均为官能团).请回答下列问题:
(其中-x、一y均为官能团).请回答下列问题: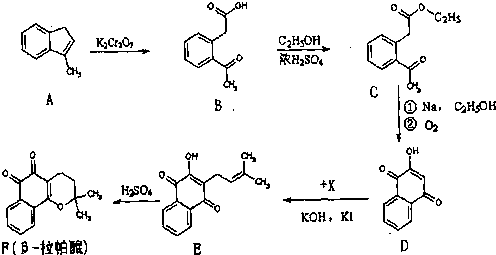
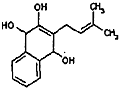 ,写出此有机物分子中含有的官能团名称:
,写出此有机物分子中含有的官能团名称: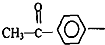 结构且能水解的所有同分异构体的结构简式:
结构且能水解的所有同分异构体的结构简式: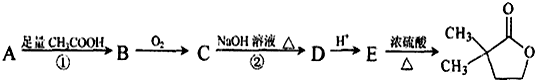
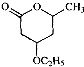 是B的一种重要的同分异构体.请设计合理方案,完成从
是B的一种重要的同分异构体.请设计合理方案,完成从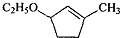 到
到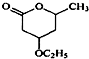 的合成路线(用流程图表示,并注明反应条件).
的合成路线(用流程图表示,并注明反应条件).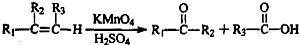 ;
;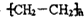 .
.