题目内容
9.下列说法正确的是( )| A. | 煤经处理变为气体燃料的过程属于物理变化 | |
| B. | 淀粉、油脂和蛋白质都是高分子化合物 | |
| C. | 乙烷和乙醇均能发生取代反应 | |
| D. | 乙酸乙酯和植物油均可水解生成乙醇 |
分析 A、化学变化是指在原子核不变的情况下,有新物质生成的变化.
B、油脂不是高分子化合物;
C、乙烷和乙醇分子中含有饱和碳原子上的氢原子,一定条件下氢原子可以被取代发生取代反应;
D、植物油属于酯类,也可水解,但水解不生成乙醇.
解答 解:A、煤的气化是煤与碳反应生成一氧化碳和氢气,属于化学变化,故A错误;
B、淀粉和蛋白质是高分子化合物,但油脂不是,故B错误;
C、乙烷和乙醇含有饱和氢,一定条件下能发生取代反应,故C正确;
D、植物油属于酯类,也可水解,水解生成甘油和高级脂肪酸,生不成乙醇,故D错误.
故选C.
点评 本题考查了煤的气化、油脂和蛋白质的水解、高锰酸钾的氧化性,题目难度不大.

练习册系列答案
相关题目
13.下列陈述I、II均正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | Fe2O3是红棕色粉末 | Fe2O3常做红色涂料 |
| B | SiO2是两性氧化物 | SiO2可和HF反应 |
| C | Al2O3难溶于水 | Al2O3可用作耐火材料 |
| D | SO2有漂白性 | SO2可使溴水褪色 |
| A. | A | B. | B | C. | C | D. | D |
20.煤炭、一氧化碳、氢气都是重要能源,已知:
①C(s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H2=-241.6kJ•mol-
③CO(g)+O2(g)═CO2(g)△H3=-283.0kJ•mol-1
④H2O(g)═H2O(l)△H4=-44kJ•mol-1
下列说法合理的是( )
①C(s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H2=-241.6kJ•mol-
③CO(g)+O2(g)═CO2(g)△H3=-283.0kJ•mol-1
④H2O(g)═H2O(l)△H4=-44kJ•mol-1
下列说法合理的是( )
| A. | 氢气的燃烧热△H=-241.6 kJ•mol-1 | |
| B. | 等质量的H2、CO完全燃烧时,CO释放的热量更多 | |
| C. | 煤的气化的热化学方程式为C(s)+H2O(g)═CO(g)+H2(g)△H=-131.1 kJ•mol-1 | |
| D. | 煤炭完全燃烧释放1967.5 kJ热量时转移20 mol电子 |
4.(1)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用.目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应.
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
则△H3与△H1、△H2之间的关系是:△H3=2△H2-△H1.
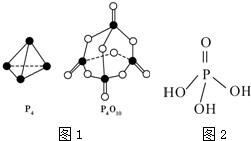
(2)白磷与氧气反应生成P4O10固体.下表所示是部分化学键的键能参数:
根据图1的分子结构和有关数据通过计算写出该反应的热化学方程式为P4(s)+5O2(g)═P4O10(s)△H=-(4c+12b-6a-5d)kJ•mol-1.
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如图2)之间脱去两个水分子产物,其结构式为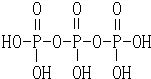 ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
(4)已知298K时白磷不完全燃烧的热化学方程式为:P4(s,白磷)+3O2(g)═P4O6(s)△H=-1 638kJ•mol-1.
在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应.则所得到的P4O10与P4O6的物质的量之比为3:1.

反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
则△H3与△H1、△H2之间的关系是:△H3=2△H2-△H1.
(2)白磷与氧气反应生成P4O10固体.下表所示是部分化学键的键能参数:
| 化学键 | P-P | P-O | P═O | O═O |
| 键能/kJ•mol-1 | a | b | c | d |
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如图2)之间脱去两个水分子产物,其结构式为
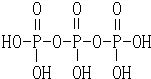 ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.(4)已知298K时白磷不完全燃烧的热化学方程式为:P4(s,白磷)+3O2(g)═P4O6(s)△H=-1 638kJ•mol-1.
在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应.则所得到的P4O10与P4O6的物质的量之比为3:1.
14.下列离子方式书写正确的是( )
| A. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2 2ClO-+CO2+H2O=2HClO+CO32- | |
| B. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3↓+3H+ | |
| C. | Na2S溶液中滴加NaClO溶液:S2-+ClO-+H2O=S↓+Cl-+2OH- | |
| D. | 将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
1.下列解释事实的离子方程式正确的是( )
| A. | 铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | 在NaClO溶液中通入过量SO2气体:ClO-+H2O+SO2═HClO+HSO3- | |
| C. | NaHCO3与少量Ca(OH)2溶液反应:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 10mL 0.5mol/L的明矾溶液与20mL 0.5mol/L的Ba(OH)2溶液混合反应:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
18.为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是( )
| 序号 | 物质 | 试剂 | 分离方法 |
| ① | 硝酸钾(氯化钠) | 蒸馏水 | 重结晶 |
| ② | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| ③ | 乙醇(水) | 金属钠 | 蒸馏 |
| ④ | NaCl溶液(Na2S) | AgCl | 过滤 |
| A. | ①③ | B. | ①④ | C. | ② | D. | ③④ |
19.由乙烯推测丙烯(CH3CH=CH2)的结构或性质正确的是( )
| A. | 分子中3个碳原子在同一直线 | B. | 分子中所有原子在同一平面上 | ||
| C. | 与氯化氢加成只生成一种产物 | D. | 能发生加聚反应 |
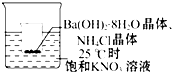 把小烧杯放入25℃的盛有饱和硝酸钾溶液的大烧杯中,小烧杯(已被设法固定)中放有 25g研成粉末的氢氧化钡晶体[Ba(OH)2•8H2O],再加入约12g的氯化铵晶体,并搅拌使其充分反应.
把小烧杯放入25℃的盛有饱和硝酸钾溶液的大烧杯中,小烧杯(已被设法固定)中放有 25g研成粉末的氢氧化钡晶体[Ba(OH)2•8H2O],再加入约12g的氯化铵晶体,并搅拌使其充分反应.