题目内容
下列各元素一定属于主族元素的是( )
| A、X元素的次外层上有18个电子 |
| B、Y元素的最外层上有2个电子 |
| C、Z元素形成的单核阳离子,具有稀有气体元素的核外电子排布 |
| D、R元素形成的单核阴离子,具有稀有气体元素的核外电子排布 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:A.第四周期的副族和ⅤⅢ族元素的次外层有18个电子;
B.原子最外层电子数等于2的还有He;
C.Cu元素能形成+1价的亚铜离子,具有稀有气体的核外电子排布;
D.单核阴离子,具有稀有气体元素的核外电子排布的只有主族元素.
B.原子最外层电子数等于2的还有He;
C.Cu元素能形成+1价的亚铜离子,具有稀有气体的核外电子排布;
D.单核阴离子,具有稀有气体元素的核外电子排布的只有主族元素.
解答:
解:A.第四周期的副族和ⅤⅢ族元素的次外层有18个电子,如Cr、V等,不是主族元素,故A错误;
B.元素原子最外层电子数等于2的还有He,属于零族元素,故B错误;
C.Cu元素能形成+1价的亚铜离子,具有稀有气体的核外电子排布,但是不属于主族元素,故C错误;
D.单核阴离子,具有稀有气体元素的核外电子排布的只有主族元素,故D正确.
故选D.
B.元素原子最外层电子数等于2的还有He,属于零族元素,故B错误;
C.Cu元素能形成+1价的亚铜离子,具有稀有气体的核外电子排布,但是不属于主族元素,故C错误;
D.单核阴离子,具有稀有气体元素的核外电子排布的只有主族元素,故D正确.
故选D.
点评:本题考查元素周期表的结构及应用,为高频考点,注意元素的化合价与元素的位置的关系即可解答,并注意利用特例来分析解答,题目难度不大.

练习册系列答案
相关题目
已知某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50mL b mol?L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物).下列说法正确的是( )
| A、若金属没有剩余,反应中转移的电子数目为2y NA | ||
| B、若金属全部溶解,则溶液中一定含有Fe3+ | ||
C、当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-
| ||
| D、若金属全部溶解,且产生336mL气体(标准状况),则b=0.3 |
镁铝合金6.3g完全溶于稀硝酸,若反应中硝酸被还原只产生4.48L(标准状况下)NO气体,在反应后的溶液中,加入足量1mol?L-1的NaOH溶液,生成沉淀的质量为( )
| A、8.7 g |
| B、7.8 g |
| C、16.5 g |
| D、4.0g |
下列说法正确的是( )
| A、一氧化碳是不稳定的氧化物,它能继续和氧气反应生成稳定的二氧化碳,故反应一定是吸热反应 |
| B、在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C、物质燃烧都需要氧气 |
| D、物质燃烧放出热量的多少与外界条件有关 |
 如图是我国“长征二号F”运载火箭发射现场.图中可以看到从火箭的下部喷射出大量的红棕色的气体,关于这种红棕色气体的认识正确的是( )
如图是我国“长征二号F”运载火箭发射现场.图中可以看到从火箭的下部喷射出大量的红棕色的气体,关于这种红棕色气体的认识正确的是( )| A、是溴蒸气,火箭发射时作氧化剂 |
| B、是二氧化氮气体,火箭发射时作还原剂 |
| C、是溴蒸气,火箭发射时作还原剂 |
| D、是二氧化氮气体,火箭发射时作氧化剂 |
下列物质间发生化学反应时,在不同情况下生成物不同的是( )
①C与O2 ②Na与O2 ③Na2CO3和HCl ④AgNO3和NH3?H2O ⑤Al2(SO4)2和Ba(OH)2 ⑥Cu和HNO3.
①C与O2 ②Na与O2 ③Na2CO3和HCl ④AgNO3和NH3?H2O ⑤Al2(SO4)2和Ba(OH)2 ⑥Cu和HNO3.
| A、仅①④ | B、仅①②④ |
| C、除⑤外 | D、全部 |
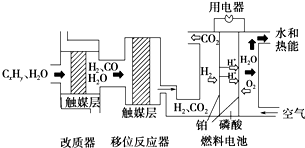 磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )| A、该系统中只存在化学能和电能的相互转化 | ||
B、在移位反应器中,反应CO(g)+H2O(g)
| ||
| C、改质器和移位反应器的作用是将CxHy转化为H2和CO2 | ||
| D、该电池正极的电极反应为O2+4H++4e-=2H2O |
