题目内容
11.标准状况下,1.12L CO有0.05molCO,有0.1mol原子,有0.1NA个原子,有0.05NA个碳原子,有0.7NA个电子.分析 根据n=$\frac{V}{{V}_{m}}$计算出1.12LCO的物质的量及含有原子的物质的量,再根据N=nNA计算出含有的原子数、碳原子数及电子数,据此进行解答.
解答 解:标准状况下,1.12L CO的物质的量为:$\frac{1.12L}{22.4L/mol}$=0.05mol,含有原子的物质的量为:0.05mol×2=0.1mol,含有的原子数为0.1NA,
0.05mol CO中含有0.05molC原子,含有0.05NA个碳原子,
0.05molCO中含有电子的物质的量为:0.05mol×14=0.7mol,含有电子数为0.7NA,
故答案为:0.05;0.1;0.1NA;0.05NA;0.7NA.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与气体摩尔体积、阿伏伽德罗常数之间的关系为解答关键,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
1.在氯化钡溶液中通入SO2,无白色沉淀产生.若将氯化钡溶液分装在两只试管中,一支加硝酸,另一支加NaOH溶液,然后再分别通入适量的SO2,结果两支试管中都有白色沉淀生成.由此得出下列结论正确的是( )
| A. | 加入NaOH,溶液pH升高,c(SO32-)增大 | B. | 氯化钡有两性 | ||
| C. | 两支试管中的白色沉淀都是BaSO4 | D. | SO2具有两性且水溶液有酸性 |
19.下列试剂可用于检验溶液中SO42-的是( )
| A. | 酚酞溶液 | B. | 硝酸银溶液和稀硝酸 | ||
| C. | 盐酸溶液 | D. | 氯化钡溶液和稀盐酸 |
6.在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,1molCuSO4能氧化P的物质的量为( )
| A. | $\frac{11}{15}$ mol | B. | $\frac{2}{5}$mol | C. | $\frac{3}{5}$mol | D. | $\frac{1}{5}$ mol |
16.同温同压下,下列各热化学方程式中反应热数值最小的是 (均为吸热反应)( )
| A. | 2A(g)+B(g)═2C(l)△H=+Q3 kJ•mol-1 | B. | 2A(g)+B(g)═2C(g)△H=+Q2 kJ•mol-1 | ||
| C. | 2A(l)+B(l)═2C(g)△H=+Q1 kJ•mol-1 | D. | 2A(l)+B(l)═2C(l)△H=+Q4 kJ•mol-1 |
3.将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体,此液体不具有的性质是( )
| A. | 光束通过该液体时形成光亮的“通路” | |
| B. | 插入石墨电极通直流电后,有一极附近液体颜色加深 | |
| C. | 向该液体中加入硝酸银溶液,无沉淀产生 | |
| D. | 向该液体中逐滴滴入过量的稀硫酸,会看到液体先生成红褐色沉淀,后沉淀溶解 |
20.下列高聚物是由两种单体缩聚而成的是( )
| A. |  | B. |  | ||
| C. | 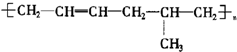 | D. | 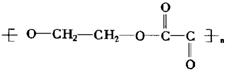 |
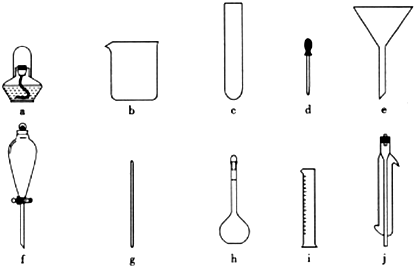
 水是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.
水是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.