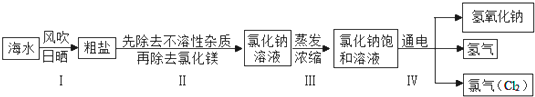
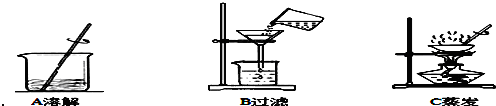
题目内容
已知NaHSO4在稀溶液中按如下方式电离:NaHSO4=Na++H++SO42-.
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,写出发生反应的离子方程式: ;在以上中性溶液中,继续滴加Ba(OH)2溶液,现象是 ;
(2)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出反应的化学方程式 .在以上溶液中,继续滴加NaHSO4溶液,写出此步反应的离子方程式: .
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,写出发生反应的离子方程式:
(2)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出反应的化学方程式
考点:离子方程式的书写
专题:离子反应专题
分析:(1)硫酸氢钠与氢氧化钡按照物质的量2:1反应,溶液显中性;继续滴加Ba(OH)2溶液,由于原溶液中硫酸根离子过量,加入氢氧化钡溶液后,发生反应:Ba2++SO42-═BaSO4↓;
(2)Ba(OH)2溶液中,逐滴加入NaHSO4溶液,硫酸氢钠少量全反应,这时氢氧根应剩余,溶液是碱性的,继续滴加硫酸氢钠溶液,氢离子与氢氧根离子反应生成水.
(2)Ba(OH)2溶液中,逐滴加入NaHSO4溶液,硫酸氢钠少量全反应,这时氢氧根应剩余,溶液是碱性的,继续滴加硫酸氢钠溶液,氢离子与氢氧根离子反应生成水.
解答:
解:(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,硫酸氢钠与氢氧化钡的物质的量之比为2:1,反应的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;在以上中性溶液中,继续滴加Ba(OH)2溶液,由于原溶液中硫酸根离子过量,加入氢氧化钡溶液后,发生反应:Ba2++SO42-═BaSO4↓,钡离子与硫酸根离子反应生成硫酸钡沉淀;
故答案为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;沉淀量增加;
(2)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液,硫酸氢钠相对于氢氧化钡量少,所以硫酸氢钠全反应,即Ba(OH)2+NaHSO4=BaSO4↓+H2O+NaOH,再和加入的硫酸氢钠中的氢离子反应,即OH-+H+=H2O;
故答案为:Ba(OH)2+NaHSO4=BaSO4↓+H2O+NaOH;OH-+H+=H2O.
故答案为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;沉淀量增加;
(2)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液,硫酸氢钠相对于氢氧化钡量少,所以硫酸氢钠全反应,即Ba(OH)2+NaHSO4=BaSO4↓+H2O+NaOH,再和加入的硫酸氢钠中的氢离子反应,即OH-+H+=H2O;
故答案为:Ba(OH)2+NaHSO4=BaSO4↓+H2O+NaOH;OH-+H+=H2O.
点评:本题考查学生离子方程式的书写,注意物质用量的多少所决定的反应产物的情况,综合性较强,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关物质的性质比较,不正确的是( )
| A、熔点:Li>Cs |
| B、还原性:F->I- |
| C、热稳定性:H2O>H2S |
| D、酸性:H3PO4>H3AsO4 |
下列说法中正确的是( )
| A、H2SO4的摩尔质量是 98 g |
| B、1 mol H2O的质量是 18 g/mol |
| C、Cl-的摩尔质量是 35.5 g/mol |
| D、1 mol N2 的体积是 22.4 L |
下列离子方程式表达正确的是( )
| A、HCO3-的水解方程式可表示为:HCO3-+H2O═H3O++CO32- |
| B、向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
| C、向NaAlO2溶液中通入过量的CO2制Al(OH)3↓2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| D、将16g铁粉投入100mL 4.0mol/L的HNO3溶液中,(还原产物只有NO)3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
用下列装置进行实验能达到相应实验目的是( )
A、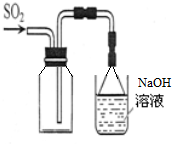 收集SO2气体 |
B、 检验产生的C2H4 |
C、 除去Fe2O3中的Fe(OH)3 |
D、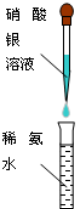 配制银氨溶液 |
下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
A、苹果酸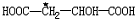 |
B、丙氨酸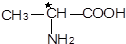 |
C、葡萄糖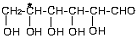 |
D、甘油醛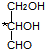 |