题目内容
对-甲基苯甲酸乙酯(F)是有机化工原料,用于合成药物的中间体.某校兴趣小组提出可以利用中学所学的简单有机物进行合成,A的产量标志着一个国家石油化工水平.其方案下:
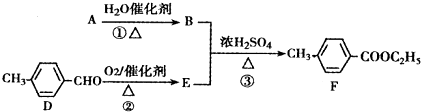
(1)写出F的分子式 ;写出E物质的名称 .
(2)指出化学反应类型:① ;③ .
(3)写出反应②的化学反应方程式: .

(1)写出F的分子式
(2)指出化学反应类型:①
(3)写出反应②的化学反应方程式:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:根据F的结构简式书写其分子式,A的产量标志着一个国家石油化工发展水平,则A为C2H4,与水发生加成反应生成B为CH3CH2OH,由F的结构可知乙醇与E发生酯化反应生成F,故E为 ,由D、E的结构可知,
,由D、E的结构可知, 中-CHO氧化为-COOH,据此解答.
中-CHO氧化为-COOH,据此解答.
 ,由D、E的结构可知,
,由D、E的结构可知, 中-CHO氧化为-COOH,据此解答.
中-CHO氧化为-COOH,据此解答.解答:
解:A的产量标志着一个国家石油化工发展水平,则A为C2H4,与水发生加成反应生成B为CH3CH2OH,由F的结构可知乙醇与E发生酯化反应生成F,故E为 ,由D、E的结构可知,
,由D、E的结构可知, 中-CHO氧化为-COOH,
中-CHO氧化为-COOH,
(1)根据F的结构简式可知其分子式为C10H12O2,E为 ,名称为:对甲基苯甲酸,故答案为:C10H12O2;对甲基苯甲酸;
,名称为:对甲基苯甲酸,故答案为:C10H12O2;对甲基苯甲酸;
(2)反应①是乙烯与水发生加成反应生成乙醇,反应③是 与乙醇发生酯化反应生成
与乙醇发生酯化反应生成 ,属于取代反应,故答案为:加成反应;酯化反应或取代反应;
,属于取代反应,故答案为:加成反应;酯化反应或取代反应;
(3)反应②的化学反应方程为:2 +O2
+O2
2 ,
,
故答案为:2 +O2
+O2
2 .
.
 ,由D、E的结构可知,
,由D、E的结构可知, 中-CHO氧化为-COOH,
中-CHO氧化为-COOH,(1)根据F的结构简式可知其分子式为C10H12O2,E为
 ,名称为:对甲基苯甲酸,故答案为:C10H12O2;对甲基苯甲酸;
,名称为:对甲基苯甲酸,故答案为:C10H12O2;对甲基苯甲酸;(2)反应①是乙烯与水发生加成反应生成乙醇,反应③是
 与乙醇发生酯化反应生成
与乙醇发生酯化反应生成 ,属于取代反应,故答案为:加成反应;酯化反应或取代反应;
,属于取代反应,故答案为:加成反应;酯化反应或取代反应;(3)反应②的化学反应方程为:2
 +O2
+O2| 催化剂 |
| △ |
 ,
,故答案为:2
 +O2
+O2| 催化剂 |
| △ |
 .
.
点评:本题考查有机物推断与合成、有机反应类型、有机方程式书写等,难度不大,掌握官能团的结构与性质是关键,注意根据转化关系中有机物结构分析.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列离子方程式书写不正确的是( )
| A、石灰乳跟稀硝酸反应:Ca(OH)2+2H+═Ca2++2H2O |
| B、铜粉投入到硝酸银溶液中:Cu+Ag+═Cu2++Ag |
| C、AlCl3溶液中加入少量的氢氧化钠:Al3++3OH-═Al(OH)3↓ |
| D、钠和冷水反应 2Na+2H2O═2Na++2OH-+H2↑ |
已知:2Fe2++Br2=2Fe3++2Br-,若向100mL FeBr2溶液中缓慢通入2.24L标况下的氯气,充分反应后,有
的Br-被氧化成Br2,则原FeBr2溶液的物质的量浓度为( )
| 1 |
| 5 |
| A、1.4mol/L |
| B、2.5mol/L |
| C、无法计算 |
| D、5.0mol/L |
已知石墨的燃烧热为△H1,金刚石的燃烧热为△H2,下列说法正确的是( )
| A、由于燃烧均为放热反应,所以石墨为重要的能源 |
| B、由于燃烧反应放热,所以△H1和△H2均取正值 |
| C、由于石墨和金刚石同为碳元素组成,所以△H1=△H2 |
| D、由于石墨和金刚石属于不同的单质,所以△H1和△H2不等 |
某温度下,在一容积固定的容器中,反应aA(g)+bB(g)═hH(g)达到平衡后,A、B、H的物质的量分别为a mol、b mol和h mol.已知a+b=2h,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是( )
| A、平衡不移动 |
| B、混合气体的密度不变 |
| C、B的体积分数增大 |
| D、a mol/L<c(A)<2a mol/L |
在一密闭容器中有如下反应:aX(g)+bY(s)?nW(g)△H=QkJ/mol.某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了曲线图:其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间.其它条件不变时,下列分析正确的是( )
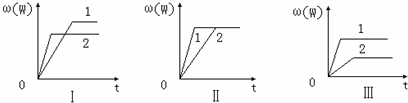

| A、图Ⅰ可能是不同压强对反应的影响,且P2>P1,a>n |
| B、图Ⅱ可能是在同温同压下催化剂对反应的影响,且2使用的催化剂效果好 |
| C、图Ⅱ可能是不同压强对反应的影响,且P1>P2,n=a+b |
| D、图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q>0 |
下列不需要用到二氧化硅的是( )
| A、光导纤维 | B、计算机芯片 |
| C、石英钟表 | D、普通玻璃 |
在无色溶液中能大量共存的离子组是( )
| A、Ca2+、Cl-、CO32- |
| B、K+、Na+、SO42- |
| C、HCO3-、Na+、OH- |
| D、K+、Fe3+、SCN- |